Chapitre 8
Épreuves prétransfusionnelles
Contexte
Les épreuves prétransfusionnelles permettent de vérifier la compatibilité entre le patient et les composants sanguins (globules rouges, plaquettes, plasma) à transfuser. Ce processus consiste à remplir la demande d’analyses de façon précise et complète, à bien identifier le patient, à prélever et à étiqueter correctement l’échantillon de sang du patient, à l’analyser en laboratoire pour déterminer le groupe sanguin et détecter la présence d’alloanticorps érythrocytaires, puis à vérifier la compatibilité. Les épreuves prétransfusionnelles sont terminées lorsqu’on a trouvé et étiqueté un composant sanguin compatible à transfuser au patient désigné. Le présent chapitre donne un aperçu des épreuves prétransfusionnelles systématiquement réalisées.
Demande d’analyses
La première étape des épreuves transfusionnelles consiste à préparer la demande d’analyses. Les renseignements concernant le patient, y compris ses nom et prénom, son numéro d’identification unique et les épreuves demandées, doivent être consignés de façon lisible. De nouvelles épreuves ne doivent pas être demandées si les résultats d’analyses du patient sont valides — conformément à ce qui est décrit dans les sections suivantes. La date et l’heure prévues de l’intervention, ainsi que la dose à transfuser, doivent être fournies si possible, de même que toute exigence et indication clinique particulières1-3.
Identification du patient et prélèvement et étiquetage de l’échantillon
Il est essentiel que les établissements hospitaliers et les services de consultation externe où l’on prélève des échantillons de sang pour les épreuves prétransfusionnelles soient dotés d’une politique et d’une procédure encadrant l’identification formelle du patient et l’étiquetage approprié des échantillons de sang prétransfusionnels. L’identité du patient doit être confirmée au moment du prélèvement des échantillons 1,3,4. La personne chargée du prélèvement doit également demander au patient de dire son prénom et son nom complets ainsi que sa date de naissance, car le bracelet d’identité qu’il porte peut ne pas être le bon4. Si l’on découvre des écarts ou des inexactitudes pendant le processus d’identification, on ne doit pas procéder au prélèvement des échantillons avant d’avoir résolu le problème de manière satisfaisante.
Les échantillons de sang utilisés pour les analyses peuvent être des échantillons traités à l’anticoagulant — EDTA de préférence — ou non, selon la politique de l’établissement. Les échantillons ne doivent pas être hémolysés. Les échantillons doivent être étiquetés en présence du patient au moment du prélèvement et identifiés au moyen du nom complet du patient ainsi qu’un numéro d’identification unique1-3, tel que le numéro de patient attribué par l’hôpital ou le numéro d’assurance-maladie provinciale. On doit également consigner la date et l’heure du prélèvement de l’échantillon ainsi que le nom du phlébotomiste 1,3,4.
Dans certaines situations, l’échantillon de sang doit être recueilli dans les 96 heures avant la transfusion. C’est le cas des patients qui ont récemment reçu une transfusion de globules rouges, des patientes qui ont été enceintes dans les trois mois précédents ou des patients dont les antécédents médicaux sont plus ou moins connus1-3. Cet échantillon peut être utilisé pour réaliser des épreuves de comptabilité croisée sur des composants sanguins jusqu’à 96 heures suivant le prélèvement. Après ce délai, comme il est possible que les patients exposés à des antigènes érythrocytaires à la suite d’une transfusion ou d’une grossesse aient développé de nouveaux anticorps, il est nécessaire de prélever un nouvel échantillon de sang et de réaliser d’autres épreuves de compatibilité pour avoir des résultats valides5.
Il arrive que l’on prélève des échantillons de sang chez des patients en pré-admission plusieurs jours ou plusieurs semaines avant la date prévue de l’intervention pour effectuer les épreuves de compatibilité croisée. Selon la politique de l’établissement, les résultats de ces épreuves peuvent être considérés comme valides au-delà de 96 heures à condition que le patient n’ait reçu aucune transfusion ou que la patiente ne soit pas tombée enceinte durant les trois mois précédents. Cela permet de s’assurer de la disponibilité d’unités de sang compatible le jour prévu de l’intervention.
Épreuves prétransfusionnelles
Les épreuves prétransfusionnelles comprennent le groupage ABO et le typage RhD des globules rouges du patient. Elles consistent également à rechercher dans son plasma des anticorps hors système ABO dirigés contre les antigènes érythrocytaires d’importance clinique. Une épreuve de compatibilité croisée, souvent appelée crossmatch, est également réalisée avant une transfusion non urgente. Il peut s’agir d’une épreuve de compatibilité croisée sérologique ou électronique.
Groupage ABO
La détermination du groupe ABO consiste à vérifier la présence des antigènes A et B sur les globules rouges du patient à l’aide d’antisérums anti-A et anti-B (épreuve globulaire) ainsi qu’à rechercher la présence d’anticorps anti-A et anti-B dans son plasma en utilisant des globules rouges du groupe A et du groupe B (épreuve sérique). Les résultats de l’épreuve globulaire doivent concorder avec ceux de l’épreuve sérique pour que le groupe ABO du patient soit validé. L’épreuve sérique n’est pas nécessaire chez les nourrissons de moins de quatre mois, car tout anticorps détecté à cette étape serait d’origine maternelle. Pour obtenir plus de renseignements sur les épreuves prétransfusionnelles chez le nouveau-né, consultez le chapitre 13.
Tableau 1 : Épreuves de groupage ABO et interprétation
|
Épreuve globulaire Globules rouges du patient testés à l’aide d’antisérum |
Épreuve sérique Plasma du patient testé au moyen de globules rouges du |
Interprétation | ||
|---|---|---|---|---|
| anti-A | anti-B | groupe A | groupe B | |
| - | - | + | + | O |
| + | - | - | + | A |
| - | + | + | - | B |
| + | + | - | - | AB |
Typage Rh
Le typage RhD consiste à analyser les globules rouges du patient pour y trouver la présence de l’antigène D au moyen de sérums anti-D. Les patients RhD négatif peuvent développer des anticorps dirigés contre l’antigène D s’ils sont exposés à des globules rouges RhD positif. Il est par conséquent préférable de transfuser des composants sanguins Rh négatif à tout receveur RhD négatif. Plus particulièrement, les enfants de sexe féminin RhD négatif et les femmes RhD négatif en âge de procréer ne doivent pas recevoir de composants sanguins RhD positif lors de transfusions ordinaires, car le développement d’anticorps anti‑D peut contribuer à la survenue de la maladie hémolytique du fœtus et du nouveau-né lors de grossesses ultérieures. Pour obtenir plus de renseignements à ce sujet, voir le chapitre 12.
Le typage ABO et Rh (technique manuelle) se fait généralement en quinze minutes.
Recherche d’anticorps
Toute personne exposée, lors d’une grossesse ou d’une transfusion, à des antigènes érythrocytaires différents des siens peut avoir dans son système des anticorps dirigés contre des antigènes non ABO. Pour détecter ces anticorps, on analyse un échantillon de plasma du patient en présence de globules rouges commerciaux du groupe O qui expriment la majorité des antigènes d’importance clinique. Pour un nourrisson de moins de quatre mois, l’analyse peut être effectuée sur son propre plasma ou sur celui de la mère.
Il existe actuellement de nombreuses techniques de recherche d’anticorps (figure 1). Certaines méthodes comprennent l’ajout de réactifs, tels que de l’albumine, une solution saline de faible force ionique ou du polyéthylèneglycol (PEG). Ces réactifs peuvent réduire la période d’incubation nécessaire et, par conséquent, le délai d’exécution de l’analyse, et aussi améliorer la sensibilité du test de dépistage d’anticorps. Certains laboratoires ont recours à la technique d’agglutination en colonne de gel avec des anticorps anti-IgG dans la colonne (carte de gel) ou des plaques de microtitrage à cupules auxquelles sont liés des antigènes érythrocytaires (en phase solide) pour le dépistage d’anticorps. Selon la technique utilisée, l’analyse prend généralement entre 30 et 60 minutes à réaliser compte tenu de la période d’incubation de l’échantillon requise.
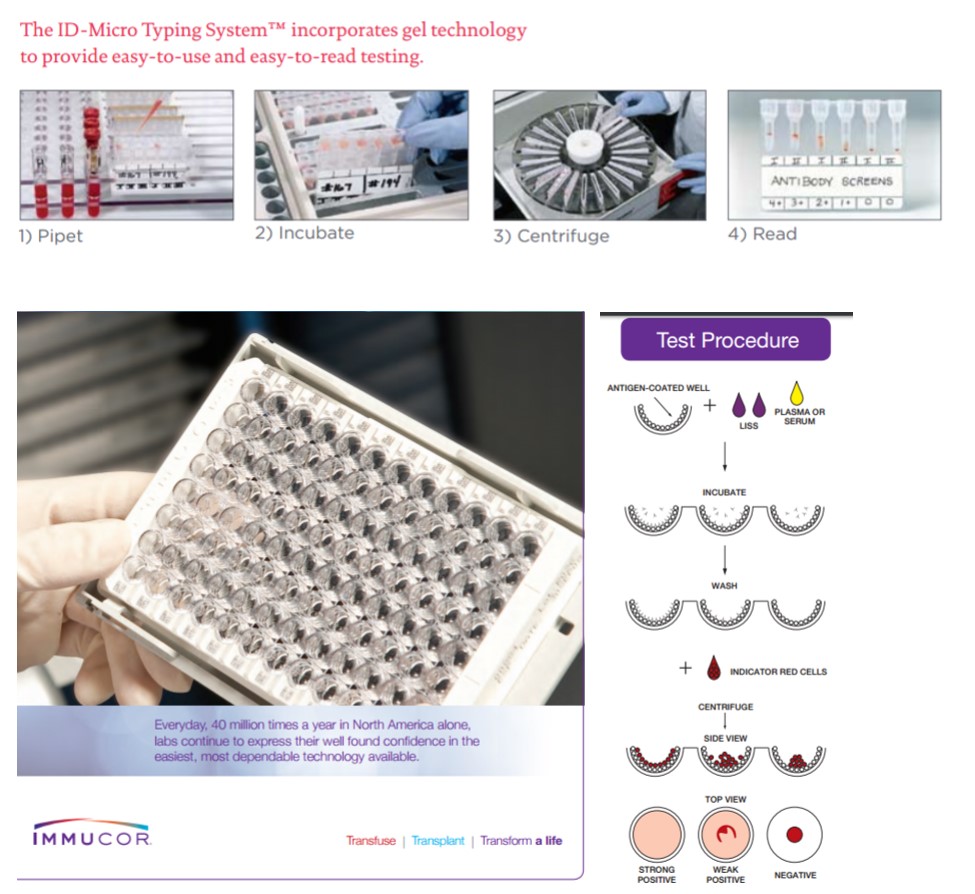
Figure 1. Exemples de trousses commerciales pour le dépistage des anticorps. Image du haut : le système de typage ID-Micro d’Ortho Clinical Diagnostics. Image du bas : Capture-R d’Immucor.
Identification des anticorps
Lorsque le test de dépistage d’anticorps révèle la présence d’un ou de plusieurs anticorps dans le plasma du patient, on procède à des analyses plus approfondies pour les identifier. Ce processus, appelé « identification des anticorps », consiste à analyser le plasma du patient à l’aide d’un panel d’hématies du groupe O dont les antigènes sont connus. L’identification comporte de multiples étapes visant à exclure ou à confirmer certains anticorps, à déterminer la température optimale de réactivité de l’anticorps et à cerner toute réactivité autologue. Le typage antigénique étendu des globules rouges d’un patient peut également contribuer à l’identification en révélant les anticorps érythrocytaires que le patient est susceptible de développer. Le temps nécessaire pour identifier les anticorps est extrêmement variable et dépend de la complexité de la recherche d’anticorps requise. Dans certains cas, le processus exige des techniques ou des antisérums qui ne sont disponibles que dans des laboratoires de référence et la recherche peut prendre plusieurs jours.
Épreuve de compatibilité croisée ou crossmatch
L’épreuve de compatibilité croisée est une méthode permettant de confirmer la compatibilité entre le patient et le donneur. Il s’agit de la dernière étape à franchir avant de délivrer des unités de globules rouges à des fins de transfusion. L’épreuve peut être effectuée de façon sérologique ou électronique. Dans la méthode sérologique, on mélange les globules rouges du donneur avec le plasma du receveur dans une éprouvette ou l’utilisation d’une plateforme similaire permettant de vérifier la compatibilité. Le crossmatch électronique (assisté par ordinateur) ne requiert aucun contact physique entre l’échantillon du donneur et celui du receveur, car un programme informatique validé sélectionne le bon composant sanguin pour un patient donné. On utilise l’épreuve de compatibilité croisée électronique seulement si le test de dépistage des anticorps du patient est négatif et s’il n’y a aucun antécédent d’anticorps d’importance clinique.
Lorsqu’un patient possède un ou plusieurs anticorps d’importance clinique, les unités sélectionnées pour l’épreuve de compatibilité croisée ne doivent pas comporter les antigènes correspondants. On doit donc choisir pour la transfusion des unités de culot globulaire qui ne contiennent pas les antigènes correspondant à l’anticorps ou aux anticorps détectés chez le patient. Pour ce faire, on peut, dans certains cas, lire l’information sur le phénotype du donneur qui figure sur l’étiquette de l’unité de culot globulaire. Dans d’autres cas, la banque de sang de l’hôpital peut déterminer le phénotype du donneur en analysant les unités, ou on peut communiquer avec la Société canadienne du sang pour obtenir des unités déjà analysées. Pour en savoir plus sur le phénotypage des globules rouges, consultez le chapitre 6.
Si l’on ne trouve pas d’unités de sang compatibles, le directeur médical du service de transfusion peut autoriser la délivrance d’unités incompatibles lorsque le besoin de transfusion l’emporte sur le risque associé à la transfusion de sang incompatible. On peut faciliter la sélection des unités les plus appropriées en choisissant une unité dont le phénotype des antigènes érythrocytaires est compatible avec celui du donneur. Selon le nombre d’anticorps présents dans le plasma du patient et leur complexité, la recherche de globules rouges compatibles peut exiger plus de temps. Dans la plupart des cas, on parvient à trouver des globules rouges allogéniques compatibles qui peuvent être transfusés sans danger.
Lorsqu’il est très difficile de trouver du sang compatible, on peut obtenir des unités de sang rare ou des unités congelées auprès de la Société canadienne du sang dans le cadre du Programme de sang rare.
Groupage sanguin et dépistage d’anticorps, ou épreuve de compatibilité croisée?
Lorsqu’une transfusion sanguine est probablement nécessaire, mais pas certaine, on demande un groupage sanguin et un dépistage d’anticorps. En revanche, lorsqu’elle est nécessaire, il faut demander au service de transfusion de réaliser une épreuve de compatibilité croisée.
Il est courant de faire une demande de « groupage et dépistage » pour qu’il y ait des unités disponibles pour les patients susceptibles d’avoir besoin d’une transfusion dans un cadre médical ou chirurgical donné. En pareil cas, le laboratoire procédera à une épreuve de groupage sanguin (ABO et typage Rh) et à un dépistage d’anticorps. Si le dépistage d’anticorps se révèle négatif et qu’on a besoin de sang, une épreuve de compatibilité croisée électronique pourra confirmer la compatibilité. Comme ce processus ne prend que quelques minutes, il n’est pas nécessaire de préparer des unités à l’avance ou d’étiqueter des unités pour un patient en particulier. Dans ce contexte, si le besoin de sang est urgent, on sélectionne une unité compatible ABO et Rh en effectuant une épreuve de compatibilité croisée électronique, puis on étiquette et on délivre l’unité à transfuser.
Lorsque la demande de groupage et de dépistage révèle la présence d’un anticorps, on doit identifier cet anticorps, sélectionner des unités dépourvues de l’antigène correspondant et réaliser un crossmatch sérologique pour qu’il y ait du sang disponible aux fins de transfusion.
Lorsqu’une transfusion sanguine est prévue pour un patient, on doit présenter une demande d’épreuve de compatibilité croisée. Cette demande doit indiquer le nombre d’unités de culot globulaire requis. En pareil cas, outre l’épreuve de compatibilité, on procédera à un groupage sanguin et à un dépistage d’anticorps, de même qu’à la préparation et à l’étiquetage des unités de culot globulaire qui seront transfusées.
L’épreuve de compatibilité peut correspondre à une épreuve de compatibilité croisée assistée par ordinateur (électronique) si le résultat du dépistage d’anticorps est négatif, ou à une épreuve de compatibilité croisée sérologique si un anticorps a été décelé.
Délivrance urgente de sang
Lorsque, en raison de l’urgence d’une transfusion, les analyses prétransfusionnelles ne peuvent être effectuées, on peut envisager de délivrer sans tarder des composants sanguins qui n’ont pas été soumis à une épreuve de compatibilité croisée. Si les épreuves de groupage ABO et de typage RhD ont été réalisées, on peut fournir des unités de sang isogroupe non soumis à une épreuve de compatibilité croisée. Si aucune épreuve n’a été amorcée au moment où le sang est requis, des unités de culot globulaire du groupe O, Rh négatif ou positif, non soumises à une épreuve de compatibilité croisée doivent être fournies. Les globules rouges du groupe O négatif doivent être réservés aux situations d’urgence impliquant des enfants de sexe féminin et des femmes en âge de procréer afin de prévenir une surutilisation des réserves déjà limitées d’unités de ce groupe. Dès que l’état du patient le permet, un échantillon de sang doit être prélevé et une analyse de compatibilité croisée doit être effectuée afin de pouvoir lui transfuser aussitôt que possible du sang isogroupe compatible.

Figure 2. Sommaire des épreuves prétransfusionnelles
Ressources complémentaires
Pour vous familiariser avec l’immuno-hématologie et les tests de compatibilité des banques de sang, consultez LearnSerology.ca, une ressource éducative en ligne conçue par des spécialistes canadiens de la médecine transfusionnelle. Le programme compte six modules, en plus d’un outil interactif qui permet d’effectuer une recherche d’anticorps à l’aide d’un panel d’échantillons.
Crédits de développement professionnel continu
Les associés et les professionnels de la santé qui participent au Programme de maintien du certificat du Collège royal des médecins et chirurgiens du Canada peuvent demander que la lecture du Guide de la pratique transfusionnelle soit reconnue comme activité de développement professionnel continu au titre de la Section 2 — Apprentissage individuel. Ces personnes peuvent réclamer 0,5 crédit par heure de lecture, jusqu’à hauteur de 30 crédits par année.
Les technologistes médicaux qui participent au Programme d’enrichissement professionnel (PEP) de la Société canadienne de science de laboratoire médical peuvent demander que la lecture du Guide de la pratique transfusionnelle soit reconnue en tant qu’activité non vérifiée.
Remerciements
L’auteure remercie Darlene Mueller, M.A., ART, et Matthew Yan, M.D., FRCPC, d’avoir effectué la révision du présent chapitre.
Suggestion de citation
Duncan J. Chapitre 8 : Épreuves prétransfusionnelles dans Clarke G, Chargé S (dir.), Guide de la pratique transfusionnelle, Ottawa, Société canadienne du sang. 2019 [cité le 10-07-2020]. Disponible sur le Web : developpementprofessionnel.sang.ca.
Si vous avez des questions ou des suggestions d’amélioration concernant le Guide de la pratique transfusionnelle, veuillez communiquer avec nous par l’entremise de notre formulaire.
Références
- Comité des normes de la SCMT. Normes pour services transfusionnels en milieu hospitalier de la SCMT, Ottawa, Société canadienne de médecine transfusionnelle, 2017.
- Groupe CSA. CAN/CSA-Z902-15 Sang et produits sanguins labiles. Publié au Canada par CSA, 2015. http://shop.csa.ca/en/canada/blood-and-blood-components/cancsa-z902-15/invt/27020812015.
- The Standards Program Committee and the Blood Banks and Transfusion Services Standards Program Unit. Standards for Blood Banks and Transfusion Services. Normes publiées par l’AABB, 2016.
- Murphy M. F., A. C. Casbard, S. Ballard, I. A. Shulman, N. Heddle, J. P. Aubuchon, S. Wendel, A. Thomson, T. Hervig, K. Downes, P. M. Carey, W. H. Dzik et BEST Research Collaborative. « Prevention of bedside errors in transfusion medicine (Probe-Tm) Study: a cluster-randomized, matched-paired clinical areas trial of a simple intervention to reduce errors in the pretransfusion bedside check », Transfusion, vol. 47, 2007, pp. 771-780. https://www.ncbi.nlm.nih.gov/pubmed/17465940.
- Shulman I. A., J. M. Nelson et R. Nakayama. « When should antibody screening tests be done for recently transfused patients? », Transfusion, vol. 30, 1990, p. 39-41. https://www.ncbi.nlm.nih.gov/pubmed/2296788.