Don d’organes et de tissus après décès dans le cas de l’aide médicale à mourir et des patients conscients et aptes – document d’orientation
Une copie PDF du rapport suivant peut vous être envoyée sur demande. Pour en faire la demande, écrivez à OTDT@blood.ca en mentionnant le titre du rapport et indiquant « Demande de document PDF » en objet.
Préface
Au Canada, le don d’organes de donneurs décédés est une pratique courante qui permet de sauver ou d’améliorer la vie de plus de 2 000 personnes chaque année, et qui représente trois transplantations sur quatre1. Le don d’organes après décès est permis après la mort, laquelle est déterminée selon des critères neurologiques ou circulatoires. Le don après un décès neurologique (DDN), le type de don le plus courant au pays, affiche un taux assez stable depuis une décennie. Le don après un décès circulatoire (DDC), longtemps considéré comme plus controversé que le DDN, devient de plus en plus courant et représentait 23 % de tous les dons d’organes au Canada en 20161. La pratique en matière de DDC évolue également. Les lignes directrices établies en 2005 concernaient le scénario classique où l’on ne s’attend pas à ce qu’un patient inconscient, inapte et gravement malade survive après l’arrêt des traitements de maintien des fonctions vitales (TMFV)2.
Toutefois, deux progrès récents ont amené de nouvelles situations dont les ramifications éthiques et pratiques ne sont pas clairement abordées dans ces lignes directrices. Premièrement, à la suite de la décision de la Cour suprême du Canada dans la cause Carter c. Canada3 et de l’adoption du projet de loi C-143,4 par le parlement canadien et du projet de loi 52 par le Québec5, les patients canadiens admissibles atteints d’une maladie terminale peuvent désormais demander de l’aide médicale à mourir (AMM) pour mettre fin à leur vie sous la supervision d’un médecin ou d’une infirmière praticienne. Deuxièmement, la volonté de faire un don d’organes est de plus en plus souvent exprimée par des patients atteints de maladies neuromusculaires dégénératives dont la vie dépend de la ventilation mécanique (effractive ou non) et qui ont pris la décision d’interrompre les traitements de maintien des fonctions vitales. Ces situations se distinguent du scénario du DDC classique puisque ces donneurs conscients et aptes peuvent exprimer eux-mêmes leur volonté de cesser les traitements de maintien des fonctions vitales et de faire don de leurs organes. Ces situations, difficiles sur le plan émotionnel et moral pour les équipes de soins, soulèvent de nouvelles questions éthiques et pratiques pour les patients, les familles, les professionnels de la santé, les institutions et la société en général.
Confrontés à ces cas individuels et aux demandes des patients, les médecins ont demandé des directives sur la façon de gérer le don d’organes chez ces patients conscients et aptes à prendre des décisions. Pour répondre à ce besoin, la Société canadienne du sang et la Fédération des sciences neurologiques du Canada, de concert avec la Société canadienne de soins intensifs, la Société canadienne de transplantation et l’Association canadienne des infirmiers/infirmières en soins intensifs, ont décidé d’étudier la question afin de fournir une orientation sur les aspects éthiques, juridiques et cliniques du don d’organes et de tissus par les patients conscients et aptes.
Sommaire
But et objectifs de l’atelier
La Société canadienne du sang a organisé un forum à Toronto, les 15 et 16 mai 2017. L’atelier de deux jours a réuni des spécialistes en médecine, en droit et en bioéthique ainsi que des patients provenant de diverses régions du Canada. Le forum visait à élaborer un document d’orientation destiné aux cliniciens, aux gestionnaires des programmes de don et des organismes de don d’organes (ODO), aux spécialistes des soins de fin de vie, aux professionnels amenés à administrer l’aide médicale à mourir (AMM) et aux responsables de l’élaboration des politiques à propos du don d’organes et de tissus par les patients conscients et aptes. Les objectifs de l’atelier étaient les suivants :
- Analyser, du point de vue juridique, médical et éthique, le don d’organes et de tissus chez le patient conscient et apte.
- Élaborer et publier un document d’orientation sur la présentation du don d’organes et de tissus aux patients ayant pris une décision qui entraîne une mort imminente :
a. patients conscients et aptes ayant décidé d’interrompre la ventilation mécanique (effractive ou non);
b. patients conscients ayant choisi d’interrompre les dispositifs de soutien extracorporel, y compris l’oxygénation extracorporelle et tout autre dispositif d’assistance circulatoire mécanique;
c. patients admissibles ayant demandé l’aide médicale à mourir (administrée au moyen d’une injection). - Élaborer une stratégie de transfert des connaissances qui inclut toutes les parties concernées.
- Recenser des pistes de recherche.
Résumé des recommandations
Don d’organes après décès par des patients conscients et aptes
1. On doit offrir aux patients médicalement acceptables, conscients et aptes ayant consenti à une intervention de fin de vie la possibilité de faire un don d’organes et de tissus. Les patients qui demandent l’aide médicale à mourir ou l’arrêt des TMFV ne doivent pas être écartés d’emblée du don d’organes et de tissus.
2. Avant de donner leur consentement à l’arrêt des TMFV ou à l’AMM, les patients, de concert avec leur médecin ou leur professionnel de la santé, doivent examiner soigneusement toutes les options de fin de vie qui s’offrent à eux.
Signalement à un organisme de don d’organes
3. Le signalement à un organisme de don d’organes doit se faire le plus tôt possible après la décision d’arrêter les TMFV ou l’admissibilité du patient à l’AMM. Si possible, une évaluation préliminaire de l’admissibilité du patient comme donneur doit être menée avant d’aborder la question du don. On évite ainsi au patient la détresse qu’il pourrait ressentir en apprenant qu’il ne peut pas faire de don pour des raisons médicales ou logistiques.
Discussions sur le don
4. La décision de demander l’AMM ou d’arrêter les TMFV doit être prise avant que la question du don ne soit abordée, et les deux processus doivent être distincts.
5. Les médecins traitants, les prestataires d’AMM et les évaluateurs en AMM doivent recevoir de la formation sur la façon de répondre aux questions sur le don d’organes. Elle doit inclure l’incidence que pourrait avoir la décision de faire un don sur les soins de fin de vie et les choix possibles, et le moment où il convient de signaler les patients à l’organisme de don d’organes. Les organismes de don d’organes doivent concevoir des listes de contrôle ou des guides de discussion afin que tous les patients reçoivent la même information et soient bien renseignés.
6. Tous les patients admissibles et acceptables sur le plan médical doivent se voir offrir la possibilité de faire un don d’organes et de tissus, conformément aux lois provinciales ou territoriales sur le signalement obligatoire, les politiques régionales et les principes éthiques du respect de l’autonomie et de l’autodétermination du patient. Cependant, le contexte doit être évalué à la lumière des valeurs et de la culture du milieu de soins. Certaines régions pourraient choisir de commencer par un système répondant uniquement aux demandes des patients.
7. Les coordonnateurs de don devront adapter la discussion de façon à garder le patient au coeur du processus d’aide médicale à mourir, ou d’arrêt des TMFV, et du don d’organes afin de préserver l’autonomie de la personne.
8. Lorsque l’on décide d’aborder le don avec le patient, la discussion doit avoir lieu de façon à lui donner suffisamment de temps pour examiner les différentes options, poser des questions et s’organiser en conséquence.
9. Il faut fournir aux patients et à leurs familles de la documentation uniforme, comme des ressources ou des brochures en ligne où ils pourront trouver des réponses à leurs questions sur le don. La décision de demander l’AMM ou de cesser les TMFV doit avoir été prise avant la discussion sur le don.
Consentement
10. Le patient doit être capable de consentir lui-même à l’AMM ou à l’arrêt des TMFV ainsi qu’au don d’organes et de tissus.
11. Les médecins, les évaluateurs en AMM et les prestataires de services pour l’arrêt des TMFV ou pour l’AMM doivent être conscients du risque de coercition ou de pressions exercées sur les patients pour qu’ils fassent don de leurs organes. Toutefois, il ne faut pas décourager une intention altruiste de don chez le patient.
12. La discussion sur le don doit respecter l’autonomie du patient, et on doit obtenir son consentement et l’honorer. Même si l’on encourage la famille à participer à la discussion sur le don, il s’agit d’abord et avant tout d’obtenir le consentement du patient, et la conversation doit rester centrée sur les besoins de ce dernier.
13. Il faut informer le patient, et s’assurer qu’il comprend bien, qu’il peut retirer son consentement à l’AMM ou au don en tout temps et que le retrait de son consentement au don n’a pas d’incidence sur son consentement ou son accès à l’AMM ou à l’arrêt des TMFV.
14. En cas de désaccord entre la famille et le patient qui souhaite donner ses organes, l’équipe de don doit tenter de résoudre le différend par le dialogue. Le consentement donné par la personne concernée doit orienter toutes les décisions subséquentes, à moins que le consentement ne soit révoqué.
15. Si un patient conscient et apte consent lui-même au don après l’arrêt des TMFV, mais qu’il perd ensuite sa capacité de prendre des décisions, il est tout à fait justifié de procéder au don après l’arrêt des TMFV, puisque le patient a été bien informé des conséquences de sa décision par un spécialiste du don et qu’il a donné son consentement dans le contexte de sa maladie et de sa mort imminente. Cependant, si un patient perd la faculté de prendre des décisions avant la procédure d’AMM, celle-ci ne peut avoir lieu.
16. L’équipe de don doit comprendre et respecter les lois et les politiques de la province en ce qui concerne la déclaration des décès résultant de l’AMM (par ex., coroner, comité spécial). Pour faciliter le don, il faut communiquer avec ces instances avant la procédure d’AMM, conformément aux lois et aux politiques en vigueur.
Tests et évaluation du donneur
17. Le médecin soignant, le personnel de l’organisme de don d’organes, les prestataires d’AMM et les équipes de transplantation doivent collaborer afin de réduire au minimum les inconvénients du don d’organes pour le patient. Exemples de mesures :
- prévoir les prises de sang à la maison;
- coordonner les tests et examens (ex. : radiographies, échographie) de façon à limiter le nombre de visites à l’hôpital et les inconvénients pour le patient.
18. Les équipes de transplantation et de chirurgie doivent établir avec l’équipe de don les examens minimums nécessaires afin d’éviter les tests inutiles.
19. Les équipes de don doivent discuter régulièrement des conséquences de résultats inattendus à des examens, notamment la découverte de maladies infectieuses non diagnostiquées, leur déclaration aux autorités de santé publique et la nécessité de retrouver toutes les personnes ayant été en contact avec le patient.
Procédure d’AMM
20. Le patient doit confirmer son consentement à l’AMM avant l’intervention. L’équipe soignante ou le prestataire d’AMM doit reconfirmer le consentement du patient avant de le déplacer ailleurs dans l’hôpital et d’entreprendre toute intervention avant le décès ayant pour but de faciliter le don. Cette étape pourrait ralentir le processus du don et réduire le risque que le patient se sente obligé de poursuivre la démarche d’AMM pour préserver la possibilité de don d’organes.
Détermination du décès
21. La règle du donneur décédé doit toujours être respectée. Les organes vitaux ne peuvent être prélevés que chez un donneur décédé, et le prélèvement ne doit pas être la cause immédiate de sa mort.
22. L’absence de pouls palpable ne constitue pas à elle seule un moyen suffisant pour déterminer le décès. Si le monitorage par cathéter artériel n’est pas possible, il faut recourir à d’autres moyens pour établir l’absence de circulation antérograde, en plus de l’absence de pouls palpable, comme une angiographie cérébrale, une échographie Doppler, une échographie de la valve aortique ou un ECG isoélectrique pour établir l’asystole.
23. Comme pour tous les cas de DDC, le décès doit être confirmé par un deuxième médecin après une période de non-intervention et d’observation continue de cinq minutes au cours de laquelle aucune intervention liée au don n’est autorisée.
Protection des patients
Séparation des décisions
24. Pour éviter tout risque de conflit d’engagement réel ou perçu, les professionnels de la santé doivent tenir séparément la discussion sur l’AMM ou l’arrêt des TMFV et celle sur le don. Les évaluateurs en AMM ne doivent pas participer aux discussions sur le don.
La discussion sur le don doit avoir lieu uniquement après que la décision d’arrêter les TMFV a été prise ou que l’admissibilité du patient à l’AMM a été établie au moyen de deux évaluations indépendantes.
25. L’équipe soignante principale doit accueillir les questions sur le don que pourrait poser le patient avant de prendre une décision concernant l’AMM ou l’arrêt des TMFV. Il est permis de fournir des renseignements généraux sur le don d’organes et de tissus après décès. Toutefois, il faut attendre que la décision d’AMM ou d’arrêt des TMFV ait été prise avant de discuter du don comme tel ou de prendre des décisions en ce sens.
26. Les patients pourraient vouloir retarder l’intervention d’AMM en raison d’une amélioration temporaire de leur santé ou d’un événement qu’ils tiennent à vivre avant de mourir. Il est important de rappeler que le patient est tout à fait libre de reporter l’intervention d’AMM et qu’il faut tenter le plus possible d’honorer sa volonté de faire un don d’organes dans un tel cas.
Don dirigé et don conditionnel
27. Aucune restriction ne peut être imposée quant au choix du receveur des organes. Chez les patients qui envisagent l’AMM ou l’arrêt des TMFV, il ne faut pas encourager ni offrir le don dirigé après le décès (où le donneur destine ses organes à un receveur en particulier) ni le don conditionnel (par ex., les organes seront donnés uniquement si le donneur peut dicter des conditions quant aux groupes sociaux qui pourront recevoir ses organes).
28. Le don de son vivant ne doit pas être offert ni encouragé chez les patients qui envisagent l’AMM ou l’arrêt des TMFV.
29. Si le patient insiste pour que son don après décès soit dirigé ou pour faire un don de son vivant, la demande doit être prise en compte. Ces demandes doivent être étudiées au cas par cas.
Séparation des rôles
30. Conformément aux lignes directrices et aux pratiques actuelles en matière de DDC, des équipes distinctes doivent s’occuper des soins de fin de vie, du don et de la transplantation. Les équipes de chirurgie responsables du prélèvement et de la transplantation ne doivent pas participer aux soins de fin de vie du patient ni à la procédure d’AMM ou à l’arrêt des TMFV. On prévoit une seule exception dans les cas où elles peuvent fournir des renseignements sur les exigences minimales quant aux investigations ou aux interventions nécessaires chez le donneur avant son décès.
31. Lorsque les patients veulent donner leurs organes après l’AMM ou l’arrêt des TMFV, mais souhaitent garder confidentielle leur décision de recourir à l’AMM ou d’arrêter les TMFV, il faut les informer du risque que leurs proches découvrent les cicatrices causées par le prélèvement de leurs organes. Il est préférable de les encourager à dévoiler leur décision à la famille. Cependant, si le patient souhaite néanmoins garder sa décision confidentielle, rien n’oblige à interrompre le processus de don.
32. Le fait qu’un donneur d’organes a bénéficié de l’AMM ne doit pas être divulgué au receveur potentiel à l’étape de l’attribution. Toutefois, il pourrait être nécessaire de divulguer des renseignements médicaux sur la maladie dont souffrait le patient, conformément aux lignes directrices régissant la distribution exceptionnelle.
Soutien au patient et à la famille
33. Des professionnels spécialement formés, comme des médecins spécialistes du don, des coordonnateurs de don, des intervenants pivots ou des travailleurs sociaux doivent être disponibles pour répondre aux questions du patient et faciliter la coordination de l’AMM ou de l’arrêt des TMFV et du don. Le processus peut s’échelonner sur plusieurs semaines. Il faut donc fournir au patient et à sa famille des instructions précises pour leur permettre d’accéder à ces ressources.
34. Le soutien doit être offert à l’endroit le plus pratique et dans le contexte le mieux adapté pour le patient; il peut s’agir de visites à domicile ou d’un soutien coordonné avec les visites à la clinique. Dans le cas des patients habitant loin, la communication par vidéo pourrait être utile.
35. L’équipe de don doit collaborer avec le patient, sa famille et le prestataire de l’AMM ou de l’arrêt des TMFV afin d’établir un plan et les meilleures options possibles pour le déroulement de l’AMM ou de l’arrêt des TMFV dans le but d’exaucer les volontés du patient, de protéger la possibilité de don et de l’arrimer à la logistique de l’établissement hospitalier.
36. Il est essentiel que le soutien soit continuellement offert aux patients et à leurs familles. Même si le patient a consenti au don, il se peut que celui-ci ne soit pas possible pour les raisons suivantes : absence de receveur compatible, détérioration de l’état du patient qui compromet son admissibilité médicale au don, anomalies découvertes au moment du prélèvement de l’organe ou retrait du consentement par le patient. Ces patients et leurs familles doivent continuer à bénéficier d’un soutien, même en l’absence de don.
37. Le soutien donné aux membres de la famille doit se poursuivre après le décès du patient. Il faut élaborer des processus pour permettre aux familles de formuler des commentaires sur leur expérience, ce qui pourrait les aider à faire leur deuil et favoriser l’amélioration de la qualité.
Sclérose latérale amyotrophique (SLA) et autres maladies neurodégénératives
38. On devrait offrir aux patients atteints de SLA ou d’autres maladies neurodégénératives non transmissibles la possibilité de faire un don d’organes après leur décès.
39. Les ODO doivent faire preuve de prudence dans l’attribution d’organes provenant de donneurs atteints de maladies neurodégénératives qui n’ont pas été diagnostiquées ou qui évoluent très rapidement, puisque celles-ci peuvent représenter un risque accru pour les receveurs. L’attribution des organes dans ce contexte doit suivre les politiques et les pratiques encadrant la distribution exceptionnelle.
40. Les spécialistes de la transplantation doivent soupeser soigneusement les avantages de l’intervention et les risques de préjudice qui pourraient découler de la greffe d’un organe provenant d’un donneur atteint d’une maladie neurologique. Le spécialiste de la transplantation doit s’appuyer sur son jugement pour aider le candidat à la transplantation à prendre une décision. Le chirurgien pourrait vouloir consulter le neurologue du donneur pour fournir une opinion plus éclairée au receveur potentiel.
41. Tous les cas de SLA ou d’autres maladies neurodégénératives qui surviennent chez des receveurs d’une transplantation doivent être signalés à Santé Canada afin de déterminer un lien potentiel avec la maladie du donneur et le risque initial d’apparition de maladies neurodégénératives chez les receveurs d’une transplantation (par ex., pour déterminer si le taux d’apparition de la SLA est le même chez les receveurs d’une transplantation que dans la population générale).
42. Les médecins qui soignent les receveurs d’organes doivent être au courant que le don provient d’un patient atteint d’une maladie neurodégénérative comme la SLA et qu’il y a un risque théorique de transmission des maladies neurodégénératives. Ils doivent également connaître les symptômes ou les plaintes qui commanderaient un examen plus approfondi par un neurologue afin d’établir la présence d’une maladie neurodégénérative.
43. La surveillance active (c.-à-d. des consultations régulières auprès d’un neurologue) n’est PAS recommandée pour les patients ayant reçu un organe d’un donneur atteint d’une maladie neurodégénérative. Le suivi neurologique impose un fardeau considérable au receveur sans lui apporter de bienfait, puisque la découverte précoce de ces maladies ne présente aucun intérêt à l’heure actuelle.
44. Des ressources d’information doivent être mises à la disposition des candidats à la transplantation et des spécialistes de la transplantation pour les aider à prendre la décision d’accepter ou de refuser un organe. Une consultation auprès d’un neurologue spécialisé dans les maladies neurodégénératives pourrait également être utile pour aider le receveur potentiel à prendre une décision éclairée. Cette information devrait également être communiquée aux ODO et aux spécialistes du don chargés d’évaluer l’admissibilité du patient qui envisage de consentir au don.
Professionnels de la santé
45. Les professionnels de la santé peuvent formuler des objections de conscience au sujet de l’AMM ou de l’arrêt des TMFV. Cependant, ils doivent tenter d’exaucer la volonté du donneur en veillant à ce que leurs objections de conscience ne privent pas le patient de la possibilité de faire un don.
46. Ils doivent agir conformément aux exigences de la province ou du territoire et à celles de leur ordre professionnel et prendre les dispositions nécessaires pour une recommandation effective.
47. Les professionnels de la santé qui soignent un patient conscient et apte ayant demandé l’AMM ou l’arrêt des TMFV doivent être mis au courant de son plan de soins de fin de vie et connaître les politiques et les procédures pertinentes.
48. Le débreffage après l’AMM ou l’arrêt des TMFV avec ou sans don doit être offert chaque fois à tous les membres concernés de l’équipe soignante. Il pourrait être utile de faire appel à une ressource externe, si cela permet aux membres de l’équipe de se sentir plus à l’aise pour parler de leur expérience.
49. Le soutien psychologique, comme celui offert par les programmes d’aide aux employés, doit être demandé au besoin. Il pourrait être avantageux que le personnel des programmes d’aide suive une formation particulière sur l’AMM, avec ou sans don, afin de mieux appuyer les professionnels de la santé concernés.
50. Les hôpitaux doivent s’assurer que le personnel en place est désireux et capable d’exaucer le souhait du patient de faire un don après son décès, sinon, qu’il dispose d’un processus de recommandation effective.
51. La participation des professionnels de la santé à l’AMM et au don d’organes chez des patients ayant reçu l’aide médicale à mourir doit demeurer volontaire, lorsque c’est possible, sans entraver l’accès aux soins pour le patient. L’équipe soignante doit être bien informée et bien préparée pour comprendre les souhaits du patient et les résultats attendus, ainsi que les politiques et les procédures pertinentes.
Rapports
52. Les cliniciens doivent être bien au fait des exigences en matière de déclaration et de production de rapports concernant l’AMM, l’arrêt des TMFV et le don dans leur province.
53. Les données relatives au don après l’AMM et aux résultats du don et de la transplantation doivent faire l’objet d’une déclaration au fédéral et être accessibles aux cliniciens, aux chercheurs et aux gestionnaires. Les résultats de la transplantation doivent pouvoir être facilement croisés avec la maladie sous-jacente du donneur ayant reçu l’AMM.
La figure 1 résume le cheminement clinique du don d’organes chez les patients conscients et aptes.
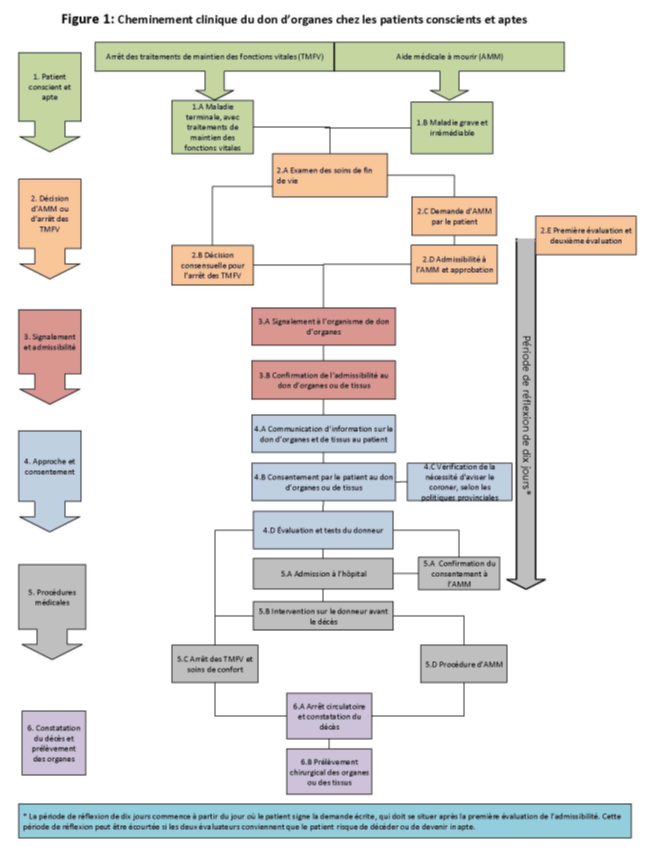
Aperçu
A. Aperçu de l’atelier
Afin de connaître le point de vue de diverses parties prenantes au pays, la Société canadienne du sang a organisé un atelier, à Toronto, les 15 et 16 mai 2017. Le forum a réuni des spécialistes en médecine, en droit et en bioéthique ainsi que des patients provenant du Canada. Il visait à élaborer un document d’orientation à l’intention des cliniciens, des gestionnaires des programmes de don et des organismes de don d’organes (ODO), des spécialistes des soins de fin de vie, des prestataires d’AMM et des responsables des politiques en ce qui concerne le don d’organes et de tissus par le patient conscient et apte. Le programme et la documentation de l’atelier se trouvent aux annexes 3 à 8 du présent rapport.
Objet et buts
1) Analyser, du point de vue juridique, médical et éthique, le don d’organes et de tissus chez le patient conscient et apte.
2) Élaborer et publier un document d’orientation sur la présentation du don d’organes et de tissus aux patients ayant pris une décision qui entraîne une mort imminente :
a. patients conscients et aptes ayant choisi d’interrompre la ventilation mécanique (effractive ou non);
b. patients conscients et aptes ayant choisi d’interrompre les dispositifs de soutien extracorporel, y compris l’oxygénation extracorporelle et tout autre dispositif d’assistance circulatoire mécanique;
c. patients admissibles ayant demandé l’AMM.
3) Élaborer une stratégie de transfert des connaissances qui inclut toutes les parties prenantes concernées.
4) Recenser des pistes de recherche.
Comité de planification et principaux contributeurs
Voici les membres du comité de planification (voir l’annexe 2 pour obtenir la liste de tous les participants à l’atelier) :
Mme Amber Appleby, Directrice associée, Société canadienne du sang
Dr Daniel Z. Buchman, Bioéthicien, Réseau universitaire de santé, Membre du Joint Centre for Bioethics, Professeur adjoint, École de santé publique Dalla Lana, Université de Toronto
Dr James Downar, coprésident
Médecin en soins critiques et en soins palliatifs, Réseau universitaire de santé et Réseau de santé Sinai
Professeur agrégé, Département de médecine, Université de Toronto
Président, Comité des affaires éthiques, Société canadienne de soins intensifs
Dre Marie-Chantal Fortin, Professeure agrégée, programme de bioéthique, Département de médecine sociale et préventive, École de santé publique de l’Université de Montréal, Chercheuse, Division de la néphrologie et de la transplantation, Centre de recherche du Centre hospitalier de l’Université de Montréal (CRCHUM), Présidente, Comité d’éthique, Société canadienne de transplantation
M. Clay Gillrie, Responsable principal de programme, Société canadienne du sang
Dre Aviva Goldberg, Néphrologue pédiatrique en chef, service de pédiatrie et de santé infantile, Université du Manitoba
Éthicienne clinique, Université du Manitoba, Directrice, Société canadienne de transplantation
Mme Vanessa Gruben, Professeure agrégée, Faculté de droit de l’Université d’Ottawa, Membre du Centre de droit, politique et éthique de la santé
Mme Jehan Lalani, Responsable de programme, Société canadienne du sang
Dr Michael D. Sharpe, coprésident
Intensiviste, Centre des sciences de la santé de London; professeur, Département d’anesthésie et de médecine périopératoire, École de médecine Schulich, Université Western Ontario
Trésorier, Société canadienne de soins intensifs
Dr Sam D. Shemie, Conseiller médical du projet, conseiller en processus et animateur de l’atelier
Division des soins intensifs pédiatriques, Hôpital de Montréal pour enfants, Centre universitaire de santé et Institut de recherche McGill
Professeur de pédiatrie, Université McGill, Conseiller médical, Don après décès, Société canadienne du sang
Dre Christen Shoesmith, Neurologue, directrice médicale, Clinique de sclérose amyotrophique latérale du Centre des sciences de la santé de London, Professeure adjointe en neurologie clinique, Université Western, Membre, Fédération des sciences neurologiques du Canada
Expert international
Dr Dirk Ysebaert, Vice-doyen, Faculté de médecine, Université d’Antwerp
Directeur, service de chirurgie hépatobiliaire et endocrinienne et de transplantation, Centre de transplantation d’Antwerp
Le Dr Ysebaert dirige le service de chirurgie hépatobiliaire et endocrinienne et de transplantation de l’hôpital universitaire d’Antwerp. Il est professeur de chirurgie au Antwerp Surgical Training, Anatomy and Research Center de la Faculté de médecine et des sciences de la santé de l’Université d’Antwerp. Il a été président et vice-président de la Belgian Transplantation Society, conseiller auprès de la European Society for Organ Transplantation et membre du conseil de la fondation internationale Eurotransplant. Il compte plus de 100 publications à son actif, portant notamment sur l’euthanasie et le don d’organes en Belgique.
Parties prenantes
Les parties prenantes sont des personnes, des groupes et des organismes ayant un intérêt particulier dans l’objet, les buts et les résultats du présent processus. Il est important d’examiner les répercussions qu’auront les déclarations de consensus sur les clientèles des parties prenantes. Dans le cadre du présent rapport, nous avons tenu compte des conséquences potentielles sur les intervenants suivants (en ordre alphabétique) :
- coroners et médecins légistes;
- autorités sanitaires, gouvernements et décideurs;
- professionnels et gestionnaires de la santé oeuvrant dans le domaine des soins critiques, de la médecine d’urgence, de la neurologie;
- professionnels de la santé qui soignent des patients mourants et gestionnaires responsables de ce secteur;
- établissements, par ex., hôpitaux, régions sanitaires;
- prestataires et évaluateurs en matière d’AMM;
- organismes de don d’organes (ODO), personnel lié au don, professionnels et gestionnaires de la santé participant au processus de don;
- partenaires pour l’élaboration de pratiques exemplaires;
- patients et société en général;
- bailleurs de fonds et organismes en recherche.
Sujets inclus
1) DDC chez les patients présentant les caractéristiques suivantes :
a. éveillés, conscients et aptes;
b. adultes ou mineurs matures;
c. capacité de consentir eux-mêmes de manière éclairée à leur propre traitement ou à la prise de décisions relatives à leurs soins de fin de vie;
d. ont choisi une intervention de fin de vie qui entraîne une mort imminente :
i. arrêt des traitements de maintien des fonctions vitales,
ii. aide médicale à mourir conforme aux lois actuelles ou à venir en la matière.
2) Pathogenèse et transmissibilité des maladies qui rendraient un patient admissible à l’AMM ou à l’arrêt des TMFV et qui auraient un effet sur son admissibilité médicale au don d’organes
3) Implications éthiques et résultats possibles découlant de l’acceptation de ces patients comme donneurs d’organes et de tissus
4) Besoins d’éducation et de formation des professionnels de la santé
5) Sensibilisation du public et des patients
Sujets exclus
1) Aspect éthique de l’AMM ou de l’arrêt des TMFV
2) Pratiques exemplaires en matière d’AMM ou d’arrêt des TMFV indépendamment du don d’organes et de tissus
3) Don par euthanasie (c.-à-d. un don d’organes contraire à la règle du donneur décédé)
4) Don d’organes provenant d’un donneur vivant
Hypothèses et principales considérations
1) Les participants à l’atelier et le public canadien appuient largement le don et la transplantation d’organes. Le don et la transplantation d’organes profitent à la société.
2) Les lignes directrices canadiennes actuelles sur le DDC contrôlé2 n’abordent pas suffisamment la gestion des patients conscients et aptes.
3) La demande de don d’organes et de tissus par des patients conscients et aptes exige un cadre d’orientation clinique, bioéthique et juridique.
4) La prestation de soins optimaux aux patients mourants constitue la priorité du milieu de la santé.
5) Les décisions prises par le patient lui-même constituent la norme la plus élevée de prise de décision en matière de traitements et de soins de fin de vie.
6) Conformément aux lois et pratiques en vigueur, le don d’organes après le décès doit respecter la règle du donneur décédé.
7) L’intégrité professionnelle doit toujours être préservée. Les prestataires de soins de santé sont guidés par leurs propres valeurs et coryances, ainsi que par les valeurs et les normes de pratique de la profession.
B. Déroulement de l’atelier
Avant l’atelier, le comité de planification a commandé un sondage, effectué des recherches dans des publications et préparé de la documentation afin d’orienter et de soutenir les discussions sur les sujets suivants :
1) attitudes des Canadiens à l’égard du don d’organes et de tissus par des patients conscients et aptes; annexe 3 – Sondage IPSOS auprès du public;
2) demandes de don d’organes par des patients conscients et aptes; annexe 4 – Gruben, Yazdami et Goldberg;
3) pathogenèse et risque de transmission de la sclérose latérale amyotrophique; annexe 5 – Shoesmith;
4) objection de conscience concernant le don après l’AMM; annexe 6 — Buchman et Gruben.
L’atelier s’articulait autour de présentations en plénière données par des cliniciens canadiens et internationaux, des éthiciens en matière de don et de transplantation d’organes, des spécialistes en droit et par un coroner ainsi que des représentants des patients. Voir l’annexe 7 pour obtenir le programme complet.
Les participants devaient discuter en petits groupes pendant l’atelier et arriver à des déclarations de consensus sur des questions de fond formulées à partir des fiches d’information et des présentations des spécialistes. Voir l’annexe 8 pour obtenir les fiches d’information et les questions de fond. Les principaux points soulevés et les conclusions obtenues au cours de ces discussions en groupes étaient ensuite présentés en plénière.
Arrêt des traitements de maintien des fonctions vitales et don après un décès circulatoire contrôlé
La plupart des cas de DDCc surviennent à la suite d’une lésion cérébrale catastrophique. Dans ces situations, le patient est inconscient et, par conséquent, incapable de participer aux décisions relatives à ses propres soins de fin de vie. Même si la décision de faire un don d’organes et de tissus peut avoir été inscrite ou indiquée à l’avance, les décisions concernant les soins de fin de vie, l’arrêt des TMFV et le don sont prises par le mandataire du patient de concert avec l’équipe soignante.
Il y a d’autres groupes de patients chez qui la maladie incurable et terminale n’est pas liée à une lésion cérébrale catastrophique. Ces patients peuvent être conscients, aptes et capables de participer activement aux décisions concernant leurs soins de fin de vie, y compris celles qui entourent l’AMM ou l’arrêt des TMFV, et de consentir au don d’organes.
Dans les unités de soins intensifs du Canada6, l’arrêt des TMFV est l’événement le plus courant à survenir avant le décès et il constitue une étape de la trajectoire clinique de presque tous les donneurs d’organes de type DDC. La décision du mandataire du patient d’arrêter les traitements s’appuie sur un pronostic défavorable, une préoccupation quant à la souffrance du patient et une piètre qualité de vie future7; elle doit correspondre aux valeurs du patient et aux souhaits qu’il a déjà exprimés.
Même si beaucoup de ces patients pourraient être admissibles au don d’organes, on observe plusieurs obstacles, notamment : l’absence d’identification du patient à titre de donneur potentiel; l’équipe soignante n’a pas abordé le mandataire pour obtenir le consentement au don, le refus du don par la famille ou le mandataire, le décès est survenu à l’extérieur du délai acceptable pour permettre la transplantation des organes et le manque de ressources en chirurgie pour le prélèvement et la transplantation des organes8. Seuls 2 % des patients qui
décèdent en milieu hospitalier peuvent être évalués comme donneurs potentiels; de ce nombre, seulement un patient sur six fera effectivement un don d’organes8.
Aide médicale à mourir
Le contexte juridique de l’AMM a évolué rapidement au pays après que la Cour suprême du Canada a déclaré inconstitutionnelles les interdictions contenues dans le Code criminel du Canada et l’adoption, par le Québec5 dans un premier temps, puis par le gouvernement fédéral4, de lois permettant l’aide médicale à mourir dans certaines circonstances. Plus précisément, le patient doit souffrir de « problèmes de santé graves et irrémédiables », définis selon les critères suivants :
a) être atteint d’une maladie, d’une affection ou d’un handicap grave et incurable;
b) doit avoir un déclin avancé et irréversible de ses capacités;
c) sa maladie, son affection, son handicap ou le déclin avancé et irréversible de ses capacités lui cause une souffrance physique ou psychologique persistante qui lui est intolérable et qui ne peut être apaisée dans des conditions que le patient juge acceptables;
d) sa mort naturelle est devenue raisonnablement prévisible compte tenu de l’ensemble de sa situation médicale, sans pour autant qu’un pronostic ait été nécessairement établi quant à son espérance de vie.1
Données préliminaires concernant l’AMM
Lorsque cet atelier a eu lieu, les statistiques sur les cas d’AMM au Canada étaient disponibles pour la période du 1er juillet 2016 au 31 décembre 2016 (pour le Québec : du 10 décembre 2015 au 31 décembre 2016); elles sont résumées dans le tableau 1. Près de la moitié des cas d’aide médicale à mourir — 463 — ont eu lieu au Québec, où une loi distincte sur les soins de fin de vie est entrée en vigueur le 10 décembre 2015, soit six mois avant la loi fédérale. Comparativement à d’autres pays9-11, l’expérience préliminaire au Canada montre une sous-représentation des patients atteints de cancer et un nombre accru de patients atteints de maladies neurologiques chroniques. Par ailleurs, le Canada affiche le plus haut taux du monde de patients atteints de sclérose en plaques12.
Il est difficile de dire si cette tendance préliminaire d’AMM chez des patients atteints de maladies neurologiques chroniques se maintiendra ou si elle n’est attribuable qu’à une surreprésentation initiale des patients atteints de maladies chroniques (autres que le cancer) qui attendaient la disponibilité de l’AMM. Les patients atteints d’un cancer terminal qui demandent l’AMM ne sont bien souvent pas admissibles comme donneurs pour des raisons médicales. Par conséquent, les patients qui forment le bassin de donneurs potentiels, parmi les personnes qui demandent l’AMM, ont des maladies sous-jacentes d’autres types.
Tableau 1. Données sur l’AMM
| Cause du décès | Pays-Bas9 | Belgique10 | États-Unis11 | Canada |
| Cancer | 79% | 80% | 80% | 57% |
| Cardiovasculaire | 4% | 4% | 3% | 11% (combiné) |
| Pulmonaire | 16% (combiné) | 5% | 4% | voir ci-dessus |
| Neurologique | voir ci-dessus | 7% | 8% | 23% |
| Autre | voir ci-dessus | 4% | 5% | 8% |
| Nbre de cas annuel (cas/million) | 3800 (224) | 2800 (247) | 100 (0.3) | 970 (27) |
* L’euthanasie est illégale aux États-Unis, et le suicide assisté est permis uniquement dans certains États; le don d’organes n’est donc pas possible.
Justification du don après l’AMM et l’arrêt des TMFV
Une analyse de la documentation montre un appui au fait d’offrir la possibilité de faire un don d’organes après leur décès aux patients demandant l’AMM et l’arrêt des TMFV. Cependant, elle révèle aussi que cela soulève des préoccupations éthiques, résumées dans le tableau 2.
Tableau 2. Arguments favorables et défavorables au don d’organes après l’AMM ou l’arrêt des TMFV (adaptation d’un document de Shaw DM13)
| Arguments favorables au don d’organes après l’AMM ou l’arrêt des TMFV |
|
| Préoccupations soulevées par le don d’organes après l’AMM ou l’arrêt des TMFV |
|
Perception du public
En septembre 2016, la Société canadienne du sang a demandé à la société IPSOS de sonder l’opinion des adultes canadiens (n = 1 006) sur le don d’organes chez les patients conscients et aptes :
- 92 % des personnes sondées approuvent le don d’organes après le décès.
- Un fort soutien a été exprimé en faveur du don d’organes par des patients conscients et aptes après l’arrêt des TMFV (87 %) ou l’AMM (80 %).
- L’opposition est beaucoup plus vive au don après l’AMM (12 %) qu’après l’arrêt des TMFV (6 %).
- Les préoccupations exprimées par les opposants au don après l’AMM ou l’arrêt des TMFV incluent :
- transmission d’une maladie (48 %);
- pression ressentie par les patients vulnérables qui les pousse à choisir l’arrêt des TMFV ou l’AMM plus tôt qu’ils ne l’auraient fait (46 %);
- pression exercée sur des personnes vulnérables pour qu’elles donnent leurs organes (43 %).
- 80 % des participants étaient d’accord pour que le don soit discuté avec tous les patients, sans égard à leur maladie ou à leurs décisions de fin de vie.
- 83 % étaient d’accord avec la nécessité de reconfirmer la décision de don d’organes avant l’administration des soins de fin de vie.
- 53 % se disaient d’accord pour que le don soit discuté APRÈS la prise de décision concernant la fin de vie.
- 25 % se disaient indécis quant à la possibilité qu’ils acceptent un organe provenant d’un donneur à la suite de l’AMM ou d’un arrêt des TMFV.
Ces résultats montrent que les Canadiens appuient largement le fait d’offrir aux patients conscients et aptes la possibilité de faire un don après l’AMM ou l’arrêt des TMFV. Cependant, une minorité de répondants s’opposent au don après l’AMM ou l’arrêt des TMFV et se disent préoccupés par le risque de transmission d’une maladie au receveur et de coercition exercée sur le donneur. Voir l’annexe 3 pour lire le rapport complet.
Don après l’AMM — premières constatations au Canada
L’Ontario, la Colombie-Britannique et le Québec comptent la plus vaste expérience en matière de don après l’AMM. En date du mois d’avril 2018, l’Ontario comptait huit dons d’organes, la Colombie-Britannique, trois, et le Québec, quatre. La Loi sur le Réseau Trillium pour le don de vie de l’Ontario exige de contacter le Réseau Trillium pour le don de vie (RTDV) lorsque le décès d’un patient est imminent29. Cette règle a été interprétée comme ayant pour effet d’obliger le signalement systématique à l’ODO de tous les patients qui s’orientent vers l’AMM30. Au Québec, la Commission de l’éthique en science et en technologie (CEST) et Transplant Québec ont d’abord émis des directives contradictoires sur l’opportunité de faire une demande de don dans ce contexte14, 31, 32. Au départ, Transplant Québec déconseillait d’aborder la question du don avec les patients qui demandaient l’AMM et préconisait d’offrir le don uniquement lorsque le patient faisait une « double demande », c’est-à-dire d’AMM et de don d’organes. Par la suite, Transplant Québec s’est ravisée et a modifié sa politique et est désormais en faveur de la présentation systématique d’une demande de don.
Parfois, certains coordonnateurs de don se sont dit à l’aise avec l’idée que le patient soit capable d’exprimer sa propre volonté et de donner son consentement au don. Toutefois, d’autres ont dit ressentir une forte tension émotionnelle dans de telles circonstances. Les transplantologues et les chirurgiens peuvent avoir des réserves d’ordre éthique à propos du don par des patients conscients et aptes après l’AMM ou l’arrêt des TMFV. L’inconfort ou une mauvaise compréhension face à de telles circonstances pourrait compromettre la transplantation.
Un autre défi réside dans l’exécution des tests pour évaluer l’admissibilité des donneurs potentiels. Ces tests (par ex., prises de sang, imagerie diagnostique) sont habituellement effectués à l’hôpital. Or, de nombreux patients conscients et aptes ne sont pas hospitalisés à cette étape et, en raison de leur maladie, ils pourraient avoir de la difficulté à se rendre à l’hôpital pour y subir les épreuves nécessaires à l’évaluation.
Les ODO ou les programmes de don, les programmes de transplantation, les éthiciens cliniques et les comités de bioéthiciens, ainsi que des cliniciens d’un peu partout au Canada ont amorcé l’élaboration de processus pour permettre aux patients conscients et aptes de faire un don après l’AMM ou l’arrêt des TMFV. Toutefois, les politiques sur l’admissibilité au don des patients atteints de maladies neurodégénératives, l’évaluation de cette admissibilité, l’acceptabilité des interventions avant le décès, la logistique et les méthodes de constatation du décès continuent de susciter des débats et demeurent des sphères de pratique en évolution.
Le don après l’euthanasie en Belgique
La Belgique a légalisé l’euthanasie en 2002, un an avant les Pays-Bas. En Belgique, pour être admissibles à l’euthanasie, les patients doivent faire état d’une souffrance physique ou psychique constante et insupportable qui ne peut être soulagée26. La loi belge stipule ceci : « le patient est majeur ou mineur émancipé, capable et conscient au moment de sa demande; la demande est formulée de manière volontaire, réfléchie et répétée, et qu’elle ne résulte pas d’une pression extérieure ».
L’une des principales différences entre la loi canadienne et belge est que cette dernière permet l’euthanasie chez les patients et chez les mineurs matures dont la maladie, y compris la maladie mentale, n’est pas terminale.
En Belgique, l’euthanasie et le don exigent des décisions distinctes par le patient et sont gérés par des équipes médicales distinctes. À l’heure actuelle, on n’aborde pas activement la question du don avec les patients par crainte qu’il y ait perception de pression ou de coercition, mais on accepte d’examiner les demandes formulées par les patients. Les discussions sur le don amorcées par les patients peuvent avoir lieu après l’acceptation de la demande d’euthanasie.
L’euthanasie doit avoir lieu dans un hôpital afin que le don et les procédures qui s’y rattachent puissent être effectués dans une salle d’opération, ou près de celle-ci, afin de réduire au minimum le temps d’ischémie. Même si on tente le plus possible d’exaucer la volonté du
patient et de sa famille et d’assurer leur confort, certains patients refusent de donner, parce qu’ils préfèrent mourir à la maison.
Lorsqu’il s’agit d’un processus de don après euthanasie, on administre de l’héparine tout de suite après les médicaments euthanasiques, et le décès est constaté par trois cliniciens. La constatation du décès est faite cliniquement sans dispositif de surveillance invasif; il n’est donc pas nécessaire de mettre en place un cathéter artériel. Une période de non-intervention de cinq minutes est observée avant le prélèvement des organes. Dans le cas d’un don de poumons, on intube et ventile le donneur après la période de non-intervention de cinq minutes. Étant donné que la combinaison de médicaments utilisée pour réaliser l’euthanasie est considérée par certains comme étant cardiotoxique, les transplantations cardiaques ne sont pas possibles à l’heure actuelle en Belgique. Des patients ont exprimé le vif désir de pouvoir donner leur coeur, et des discussions ont cours, dans un souci de respect de l’autonomie du patient, pour élaborer des stratégies qui rendraient possible le don de coeur.
En 2015, l’euthanasie représentait 2 022 décès sur 110 508 (1,8 %) en Belgique, et on comptait huit donneurs après euthanasie, soit 2,5 % de tous les donneurs après un décès. Environ 75 % des patients ayant reçu l’euthanasie étaient atteints d’une affection maligne en phase terminale; ceux-ci n’étaient donc pas admissibles au don. De 2005 à 2015, 23 patients, dont l’âge moyen était de 49,3 ans, sont devenus donneurs d’organes après l’euthanasie. Les maladies sous-jacentes de ces patients se répartissaient comme suit : troubles neuropsychiatriques (n = 7), AVC ou hémorragie (n = 4), sclérose en plaques (n = 5), autres maladies neurodégénératives (n = 10) et douleur insupportable (n = 2). Le délai moyen avant l’arrêt circulatoire était de 7,9 minutes, et le délai moyen de mise en route de la perfusion était de 19,4 minutes après l’arrêt circulatoire33.
Jusqu’à 2015, 92 organes provenant de 23 donneurs (45 reins, 21 foies, 16 poumons et 10 îlots) ont été transplantés; la qualité des organes des patients décédés par euthanasie était très bonne. Certains tissus ont également été greffés; cependant, dans certains cas, des inquiétudes quant au risque de transmission de la maladie neurologique ont limité le nombre de greffes de tissus.
Politiques internationales concernant le don après un décès découlant de l’AMM
Même si l’aide médicale à mourir est désormais autorisée dans plusieurs pays, le don après décès dans ces cas n’est pas permis dans tous les pays. Voir le tableau 3. En Suisse, le suicide assisté est légal, mais le don après le décès dans de telles circonstances est impossible, en partie parce que le geste est posé par une personne qui n’est pas médecin et ailleurs qu’à l’hôpital. Les lois du Luxembourg précisent que les organes peuvent être prélevés uniquement après l’arrêt des traitements en raison de lésions trop importantes au cerveau. Par conséquent, les patients conscients et aptes ne peuvent consentir au don après décès.
Tableau 3 : Politiques sur le don d’organes dans les pays où le décès avec assistance médicale est permis (adapté de la publication des chercheurs Allard et Fortin, J Med Ethics, 2017)
| Pays ou État | Politique sur le don d’organes |
| Suisse (suicide assisté avec l’aide d’une personne non médecin) | Pas possible |
| Belgique (euthanasie) | Possible à la demande du patient33 |
| Pays-Bas (euthanasie, suicide assisté) | Possible après l’euthanasie à la demande du patient Protocole officiel de don après euthanasie en cours de préparation27 |
| Luxembourg (euthanasie) | Illégal |
| États de l’Oregon, de Washington, du Vermont et du Montana (États-Unis) (suicide assisté) | Pas possible |
| Ontario, Canada | Option de don offerte systématiquement |
| Québec, Canada | Au début, à la demande du patient Demande systématique dorénavant |
Une copie PDF du rapport complet peut vous être envoyée sur demande. Pour en faire la demande, écrivez à OTDT@blood.ca en mentionnant le titre du rapport et indiquant « Demande de document PDF » en objet.
Remerciements
Le présent document d’orientation est dédié aux Dres Shelly Sarwal et Linda Panaro qui ont proposé des perspectives uniques et des réflexions judicieuses pendant son élaboration. Par leurs connaissances et leur volonté de sensibilisation, elles ont guidé l’atelier en plus de contribuer à la rédaction de ce document qui orientera la pratique et favorisera l’élaboration de politiques tant à l’échelle provinciale que nationale.
Le comité de planification souhaite également remercier tous les patients qui ont envisagé, en fin de vie, le don d’organes après l’aide médicale à mourir ou l’arrêt des traitements de maintien des fonctions vitales.
© Société canadienne du sang, 2018. Tous droits réservés.
Des portions du présent document peuvent être commentées, reproduites ou traduites à des fins de formation, de recherche ou d’étude privée, mais ne peuvent être mises en vente ni utilisées dans un but commercial. Toute utilisation de l’information doit préciser que la Société canadienne du sang en est la source. Tout autre usage de cette publication est strictement interdit sans la permission de la Société canadienne du sang.
La Société canadienne du sang n’assume aucune responsabilité quant aux conséquences, aux pertes, aux blessures, prévues ou non, qui pourraient découler de la mise en oeuvre, de l’utilisation, bonne ou mauvaise, de l’information ou des recommandations contenues dans le présent rapport. Celui-ci contient des recommandations qui doivent être évaluées à la lumière des exigences médicales, juridiques et éthiques pertinentes et propres à chaque cas.
La production de ce rapport a bénéficié de contributions financières de Santé Canada, et des gouvernements provinciaux et territoriaux. Les opinions qui y sont exprimées ne reflètent pas nécessairement celles des gouvernements fédéral, provinciaux ou territoriaux.