Réactions transfusionnelles anaphylactiques et déficit en IgA
Auteures : Aditi Khandelwal, MDCM, FRCPC; Gwen Clarke, MD, FRCPC; Mindy Goldman, MD, FRCPC
Date de publication : mai 2021
Dates de publication en ligne précédentes : mars 2012, mis à jour en juillet 2018
Principaux points
- Le nombre de réactions anaphylactiques ou de réactions allergiques graves déclarées varie entre 1,2 et 5,9 pour 100 000 unités transfusées. Les données de surveillance les plus récentes de la Société canadienne du sang sur les réactions allergiques sont présentées dans son rapport de surveillance annuel.
- Divers mécanismes peuvent conduire à une réaction anaphylactique ou à une réaction allergique grave, et certaines réactions peuvent ne pas être évitables même si l’on change de produit.
- Même en présence d’anticorps anti-IgA et d’un faible taux d’IgA, le risque de réaction transfusionnelle anaphylactique est peu élevé.
- Le dépistage d’anticorps anti-IgA est recommandé seulement chez certains individus qui ont déjà eu une réaction transfusionnelle anaphylactique ou deux réactions transfusionnelles allergiques graves.
- Le formulaire (en anglais) permettant de demander le dosage d’anti-IgA est accessible sur le site Web de la Société canadienne du sang.
- Un guide proposant des directives et des conseils sur la déclaration de réactions transfusionnelles indésirables peut être consulté sur le site Web consacré au développement professionnel de la Société canadienne du sang.
Réactions transfusionnelles anaphylactiques
Définition
Selon l’International Society of Blood Transfusion (ISBT) et l’International Haemovigilance Network (IHN), on parle de réaction anaphylactique lorsque l’on est en présence de symptômes mucocutanés (démangeaisons, urticaire, gonflement des lèvres, rougeur et boursouflures autour des yeux et sur la conjonctive) accompagnés d’une obstruction des voies respiratoires supérieures ou inférieures ou d’une forte hypotension survenant pendant ou peu de temps après une transfusion.1 Ce type de réaction est souvent mortelle. Une réaction allergique est qualifiée de grave lorsque l’on observe les signes cliniques suivants : hypotension, dyspnée ou toux, tachycardie, bouffées vasomotrices généralisées ou anxiété, nausées ou vomissements, urticaire couvrant plus des deux tiers de la surface du corps.2,3,4,5 La définition d’une réaction allergique grave varie légèrement selon le programme d’hémovigilance.1,6,7
Fréquence
La fréquence des réactions transfusionnelles anaphylactiques varie d’un programme d’hémovigilance à l’autre, selon la définition précise qui lui est donnée. En général, cette fréquence s’avère d’autant plus élevée que le volume plasmatique des composants transfusés est important. Le système de surveillance des incidents transfusionnels (SSIT) de l’Agence de santé publique du Canada a déclaré 5,9 réactions allergiques graves pour 100 000 unités transfusées entre 2009 et 2013.8 Il s’agit là d’une surestimation du risque réel de réactions allergiques graves, car cela englobe des cas pour lesquels la relation avec la transfusion s’est avérée douteuse. En 2018, le système d’hémovigilance néerlandais (TRIP) a signalé 58 réactions anaphylactiques pour 494 720 composants transfusés (soit 1,2 réaction pour 100 000 unités).6 Au Royaume-Uni, le programme d’hémovigilance Serious Hazards of Transfusion (SHOT) a recensé 166 réactions allergiques graves entre 2016 et 2019 inclusivement pour un total de plus de 9,5 millions de composants sanguins (culot globulaire, plaquettes, plasma frais congelé, plasma frais congelé traité par solvant-détergent et cryoprécipité) distribués aux hôpitaux (soit 1,5 réaction pour 100 000 unités transfusées)7.
En résumé, des réactions anaphylactiques ou allergiques graves surviennent à une fréquence comprise entre 1,2 et 5,9 pour 100 000 unités transfusées selon les programmes d’hémovigilance. Il est possible que toutes les réactions ne soient pas signalées ou qu’elles ne fassent pas l’objet d’une investigation visant à déterminer si le patient présente un déficit en IgA et s’il possède des anticorps anti-IgA.
Description clinique
Une réaction anaphylactique ou une réaction allergique grave peut survenir après la perfusion d’une petite quantité de sang. Les symptômes, pouvant être bénins au départ, peuvent évoluer rapidement vers la perte de conscience, le choc distributif et, dans de rares cas, la mort. Ces réactions surviennent généralement entre 1 et 45 minutes après le début de la transfusion, bien que des réactions allergiques moins graves puissent apparaître après 2 à 3 heures.1 Les réactions anaphylactiques ou réactions allergiques graves peuvent se distinguer d’autres réactions transfusionnelles graves, comme celles dues à une contamination bactérienne, ou de réactions transfusionnelles hémolytiques aiguës par des manifestations cliniques telles que la présence de lésions cutanées, l’absence de fièvre ou de frissons et l’apparition de troubles respiratoires graves. Le tableau 1 présente les signes et symptômes qui accompagnent la réaction transfusionnelle anaphylactique.
| Appareil cutané |
|
| Appareil respiratoire |
|
| Appareil digestif |
|
| Appareil cardiovasculaire |
|
| Symptômes divers |
|
Mécanisme
Bien qu’ils soient encore méconnus, les mécanismes de la réaction transfusionnelle anaphylactique comprennent :9
- la présence d’un allergène dans le composant sanguin, auquel le receveur est sensibilisé;
- un anticorps IgE préformé du donneur dirigé contre des allergènes auxquels le receveur pourrait avoir été exposé;
- des modificateurs de la réponse biologique, comme le C3d, qui s’accumulent pendant l’entreposage de composants sanguins;
- l’exposition accidentelle et concomitante du receveur de la transfusion à un autre allergène.
Les réactions à médiation IgE sont appelées réactions d’hypersensibilité immédiates de type I. Les IgE peuvent se lier au fragment Fc des récepteurs membranaires des mastocytes et des basophiles tissulaires. Lorsque le patient est réexposé à un antigène (allergène) reconnu par les IgE qui recouvrent les mastocytes, ces derniers sont activés. Ce phénomène entraîne la réticulation des IgE liées aux récepteurs, ce qui provoque la dégranulation mastocytaire et la libération de médiateurs préformés ou néoformés de la réaction allergique.
L’histamine est le principal médiateur préformé. Elle entraîne la vasodilatation, l’augmentation de la perméabilité vasculaire, l’augmentation des sécrétions nasales et bronchiques et la contraction des muscles lisses. D’autres médiateurs granulés de la réaction allergique sont l’héparine, des enzymes, des leucotriènes, des cytokines et divers facteurs d’activation tels que les chimiokines pour les polynucléaires éosinophiles et neutrophiles et le facteur d’activation des plaquettes.
Dans la majorité des cas, l’étiologie de ces réactions est inconnue. Souvent, les patients transfusés peuvent aussi être exposés de manière concomitante à d’autres médicaments ou à des aliments qui ont pu provoquer la réaction. De rares études de cas ont mis en évidence le transfert passif d’anticorps IgE dirigés contre des antigènes d’arachide d’un donneur vers des receveurs qui ont par la suite développé une allergie aux arachides. En outre, certains receveurs peuvent présenter une carence en protéines sériques ou différents allotypes de protéines sériques comme l’haptoglobine.
Déficit en haptoglobine
Le déficit en haptoglobine s’observe plus fréquemment chez certains groupes ethniques comme les Chinois Han (1 cas sur 1 000), les Coréens (1 cas sur 1 500) et les Japonais (1 cas sur 4 000).10 Au Japon, 1,6 % des réactions transfusionnelles anaphylactiques sont attribuables à la présence d’anticorps anti-haptoglobine chez les personnes ayant un déficit en haptoglobine.11 Un cas de transfert par voie transfusionnelle de l’allergène d’arachide chez un receveur souffrant d’une grave allergie à cet aliment a également été signalé. La prédisposition atopique d’un receveur de sang, confirmée par une élévation des IgE totales et des IgE spécifiques de pneumallergènes tels que les pollens, a été associée à une incidence accrue de réactions allergiques post-transfusionnelles, mais pas nécessairement de réactions anaphylactiques.3,12
Déficit en IgA
Le déficit en immunoglobulines A (IgA) est le plus répandu des déficits immunitaires humains. Bien que la plupart des sujets déficients en IgA soient asymptomatiques, certains d’entre eux ont une prévalence plus élevée d’infections respiratoires et gastro-intestinales. Du point de vue de la médecine transfusionnelle, la présence d’anticorps anti-IgA chez un receveur déficient en IgA est une cause possible de réaction transfusionnelle anaphylactique. Environ 1 à 5 % des réactions transfusionnelles anaphylactiques dans la population caucasienne pourraient être liées à la présence d’anticorps anti-IgA chez des receveurs déficients en IgA.3,13
Investigation auprès des patients ayant eu une réaction transfusionnelle anaphylactique
Lorsqu’un patient connaît une réaction anaphylactique lors d’une transfusion, il est nécessaire de faire une évaluation complète pour déterminer les causes transfusionnelles de l’anaphylaxie et les causes non transfusionnelles.
Selon le scénario clinique, les tests de dépistage peuvent inclure un test de quantification des immunoglobulines pour connaître le taux d’IgA et le taux d’haptoglobine. Si, d’après le test de quantification des immunoglobulines, le patient semble avoir un déficit en IgA, des échantillons de son sang doivent être envoyés à la Société canadienne du sang afin qu’elle détermine s’il y a présence d’anticorps anti-IgA.
Interprétation du taux d’IgA
Le taux normal d’IgA est compris entre 100 et 600 mg/dl.1 Cependant, de nombreux individus ayant un taux d’IgA inférieur n’ont pas de véritable carence. Des tests courants de quantification des immunoglobulines peuvent être utilisés comme tests de dépistage pour identifier les individus ayant un taux d’IgA inférieur à 2-4 mg/dl. Il faut toutefois un test plus sensible, un essai immunoenzymatique (ELISA), dont la sensibilité est de 0,02 mg/dl, pour identifier les sujets atteints d’un réel déficit en IgA. Seules les personnes ayant une véritable carence en IgA (c.-à-d. un taux inférieur à 0,05 mg/dl) peuvent développer des anticorps anti-IgA.
Des tests de dépistage effectués par la Société canadienne du sang sur environ 100 000 échantillons ont permis d’identifier 139 donneurs ayant un taux d’IgA confirmé inférieur à 0,05 mg/dl.14,15 Compte tenu du nombre de donneurs, la Société canadienne du sang estime qu’environ 1 de ses donneurs sur 300 présente un déficit grave en IgA. Une analyse de quelque 39 000 échantillons de sang réalisée par Héma-Québec a révélé la présence d’un déficit en IgA chez 73 donneurs, soit une fréquence de 1 sur 531.16
Fréquence et signification clinique de la présence d’anticorps anti-IgA
Donneurs de sang
Le programme de sélection des donneurs de sang de la Société canadienne du sang a permis de déceler des anticorps anti-IgA chez 41 % des donneurs atteints d’un déficit grave en IgA.15 Dans le cadre du programme d’Héma-Québec, 53 % des donneurs gravement déficients en IgA étaient porteurs d’anticorps anti-IgA.5 Un grand nombre de ces anticorps sont fabriqués naturellement. Parmi les donneurs d’Héma-Québec, seuls 9 des 39 porteurs d’anticorps anti-IgA avaient déjà reçu une transfusion ou étaient des femmes ayant eu une grossesse.
Receveurs ayant eu une réaction transfusionnelle anaphylactique
À la Société canadienne du sang, les 0 à 4 réactions transfusionnelles anaphylactiques recensées chaque année sont probablement associées à la présence d’anticorps anti-IgA. En 2015, aucun des 12 patients ayant fait l’objet d’une investigation pour avoir eu une réaction transfusionnelle anaphylactique ne possédait d’anti-IgA, et en 2016, 1 patient sur les 9 considérés possédait des anti-IgA.17 Héma-Québec recense chaque année de 0 à 1 réaction anaphylactique attribuable à des anti-IgA.18 Dans la base de données du programme SHOT du Royaume-Uni, de 2010 à 2015 (soit en 6 ans), sur 120 cas de réactions transfusionnelles aiguës recensés en lien avec des tests de dépistage des IgA, 8 ont été associés à la présence d’anticorps anti-IgA (communication personnelle, Paula-Bolton-Maggs, novembre 2016).7 Selon la base de données TRIP,6 de 2003 à 2018, seulement 5 (0,7 %) réactions allergiques graves ou réactions anaphylactiques ont été observées chez les sujets ayant un déficit en IgA et des anticorps anti-IgA.
Si la fréquence des déficits en IgA et des anticorps anti-IgA était similaire chez les receveurs et les donneurs, on s’attendrait à ce que 1 à 1,6 patient sur 1 000 au Canada soit déficient en IgA et possède des anticorps anti-IgA. Or, la fréquence des réactions transfusionnelles anaphylactiques imputables aux anti-IgA étant inférieure à 1 pour 500 000 composants sanguins transfusés annuellement, ces réactions ne semblent pas être causées par la vaste majorité des anticorps anti-IgA. En outre, un examen de la base de données du programme d’hémovigilance français a révélé que sur 12 patients qui avaient des antécédents de réactions anaphylactiques et présentaient un déficit absolu en IgA et des anticorps anti-IgA, seulement un patient a eu une réaction allergique lors d’une transfusion ultérieure.19 Dans une étude portant sur 229 patients ayant eu une réaction allergique à une transfusion, seul 1,3 % avaient un déficit absolu en IgA et des anticorps anti-IgA.20 Ainsi, même en présence d’anticorps anti-IgA chez le receveur, le risque de réaction allergique grave ou de réaction transfusionnelle anaphylactique est faible.
Dépistage des anticorps anti-IgA chez les patients
Les patients qui ont eu une réaction anaphylactique ou deux réactions allergiques graves lors de transfusions peuvent bénéficier de tests plus poussés pour mesurer le taux d’IgA et les anticorps anti-IgA. Cependant, en ce qui concerne les patients qui semblent avoir un faible taux d’IgA et n’ont pas reçu de transfusion ou les patients qui n’ont pas eu de réaction transfusionnelle, l’utilité de ces tests n’est pas claire.21-23 Compte tenu de la fréquence élevée d’anticorps anti-IgA chez les patients et de la faible incidence des réactions transfusionnelles anaphylactiques imputables à la présence d’anti-IgA, on estime qu’environ 1 patient sur 100 qui est déficient en IgA et possède des anti-IgA présentera une réaction transfusionnelle. Aucun test ne permet à ce jour de caractériser les anticorps anti-IgA qui jouent un rôle important sur le plan clinique. Un résultat positif chez un patient pour qui un dépistage des anticorps anti-IgA n’est pas indiqué peut retarder la transfusion inutilement à cause de l’incertitude quant au besoin d’un produit spécialisé, ou peut entraîner une hésitation clinique à transfuser par peur de provoquer une réaction transfusionnelle. Par conséquent, la majorité des praticiens recommandent de ne pas faire un dosage des anticorps anti-IgA chez les patients présentant une faible concentration d’IgA s’ils n’ont pas d’antécédent connu de réaction transfusionnelle anaphylactique ou de réactions allergiques graves (2 incidents).21 De plus, si des tests réalisés antérieurement ont montré des concentrations détectables d’IgA et aucune concentration détectable d’anticorps anti-IgA, il n’est pas recommandé de faire d’autres tests relatifs aux anticorps anti-IgA.
À la Société canadienne du sang, la détection des anticorps anti-IgA peut être envisagée dans les cas suivants (voir la figure 1) :
- un patient ayant déjà eu une réaction transfusionnelle anaphylactique et ayant un taux d’IgA nettement faible ou absent;
- un patient ayant eu au moins deux réactions transfusionnelles allergiques graves ne répondant pas tout à fait à la définition de l’anaphylaxie.
La Société canadienne du sang ne réalise plus d’études quantitatives pour les IgA avant d’envoyer les échantillons pour le dépistage d’anticorps anti-IgA. Il est recommandé de déterminer s’il y a un déficit en IgA au moyen de tests effectués en milieu hospitalier. Pour le dépistage des anticorps anti-IgA, les laboratoires des hôpitaux envoient un échantillon congelé du sérum du patient avant transfusion (tube à bouchon rouge ou tube SST) à la Société canadienne du sang. Cet échantillon est ensuite expédié à un laboratoire externe qui effectue les tests. Le test utilisé est l’ELISA. Il faut un volume minimal de 0,5 ml pour pouvoir détecter des anticorps polyclonaux humains anti-IgA. Les spécimens congelés doivent être analysés dans un délai de 30 jours suivant leur congélation. Le résultat est considéré comme positif lorsqu’une concentration d’anticorps anti-IgA supérieure ou égale à 99 U/ml est détectée. Le délai d’exécution de ce test peut aller jusqu’à 15 jours.
Pour demander un dosage des anticorps anti-IgA pour un patient, veuillez utiliser le formulaire normalisé accessible sur le site Web de la Société canadienne du sang : https://www.blood.ca/fr/requisitions-and-forms
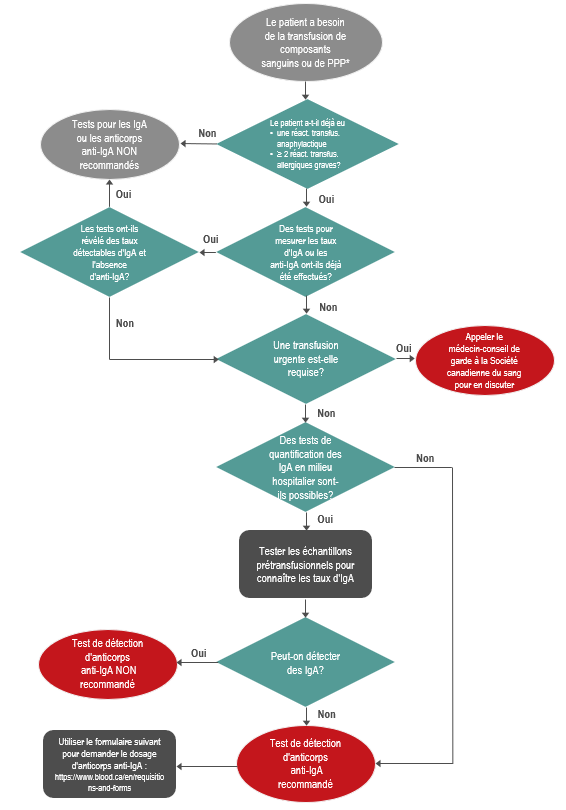
Figure 1 : Algorithme clinique à l’intention des clients de la Société canadienne du sang pour aider à la prise de décisions concernant la détection d’IgA et d’anticorps anti-IgA chez les patients ayant besoin d’une thérapie transfusionnelle.
* PPP = produit plasmatique
Recours à la transfusion chez les patients ayant déjà eu une réaction transfusionnelle anaphylactique
Chez les patients ayant des antécédents de réaction transfusionnelle anaphylactique, il est préférable de mener une enquête afin de déterminer s’ils sont porteurs d’anticorps anti-IgA. Les modalités de transfusion des patients possédant des anticorps anti-IgA et ayant eu une réaction transfusionnelle anaphylactique sont décrites dans le tableau 2. Si le patient ne présente pas de déficit en IgA ou qu’il n’a pas d’anticorps anti-IgA, et qu’il n’a manifesté qu’une seule réaction anaphylactique auparavant, la transfusion de composants sanguins non lavés peut être tentée dans des conditions contrôlées incluant l’obtention du consentement éclairé du patient, l’administration d’une prémédication et une étroite supervision médicale. Si une nouvelle réaction anaphylactique se produit, il convient de transfuser au patient des composants sanguins lavés afin d’éliminer la plus grande quantité de plasma possible.3,24 En ce qui concerne les culots globulaires, un double lavage (appelé aussi lavage supplémentaire) à l’aide d’un système automatisé est nécessaire afin de réduire le taux d’IgA à moins de 0,05 mg/dl (voir le chapitre 15 du Guide de la pratique transfusionnelle pour en savoir plus sur les composants sanguins lavés).24 Si le dosage des anticorps anti-IgA ne peut pas être effectué à temps, les modalités de prise en charge du patient doivent être établies avec le médecin-conseil de la Société canadienne du sang.
Si l’on détermine que l’étiologie d’une réaction transfusionnelle anaphylactique (ou de deux réactions graves) est un déficit en haptoglobine, des produits spécialisés peuvent être requis pour le soutien transfusionnel. Pour la transfusion de globules rouges, des culots globulaires lavés peuvent être utilisés. Par contre, pour les plaquettes et le plasma, il peut être nécessaire d’importer des produits de centres de transfusion étrangers qui ont des donneurs déficients en haptoglobine dans leur registre. Le processus d’importation de produits sanguins spécialisés peut prendre plusieurs semaines, et ces cas doivent être examinés par un médecin-conseil de garde à la Société canadienne du sang ou par le Programme de sang rare.
| Culot globulaire |
|
| Plaquettes |
|
| Plasma frais congelé, plasma congelé |
|
| Cryoprécipité |
|
| Produits dérivés du plasma (IgIV, albumine et immunoglobulines anti-Rh) |
|
Ressources de la Société canadienne du sang
- Lettre aux clients publiée le 22 janvier 2018 (accessible à sang.ca)
- Test de détection d’anticorps anti-IgA (Foire aux questions) (accessible à sang.ca) (en anglais)
- Demande de dosage de l’anticorps anti-IgA pour un patient, Formulaire F800014 (accessible à sang.ca) (en anglais)
- Algorithme clinique. Imprimer l’algorithme pour aider à la prise de décisions concernant la détection d’IgA et d’anticorps anti-IgA chez les patients ayant besoin d’une thérapie transfusionnelle.
Références
1. International Society of Blood Transfusion-Working Party on Haemovigilance. Appendix B, Proposed Standard Definitions for Surveillance of Non Infectious Adverse Transfusion Reactions. In Hemovigilance: An Effective Tool for Improving Transfusion Safety. Edited by De Vries R, Faber J. Published by John Wiley & Sons, Ltd., 2011. https://onlinelibrary.wiley.com/doi/pdf/10.1002/9781118338179.app2.
2. Callum JL, Pinkerton PH, Lima A, Lin Y, Karkouti K, Lieberman L, Pendergrast JM, Robitaille N, Tinmouth AT, Webert KE. Sang difficulté 4 : Transfusions sanguines, alternatives et réactions transfusionnelles. Publié en Ontario (Canada) par le Réseau régional ontarien de coordination du sang, 2016. https://transfusionontario.org/fr/sang-difficulte-4-transfusions-sanguines-alternatives-et-reactions-transfusionnelles-guide-de-medecine-transfusionnelle-4e-edition/.
3. Vamvakas E. Allergic and Anaphylactic Reactions. In: Transfusion Reactions, 4th Edition, edited by Popovsky M., Published in Arlington, VA, by AABB Press, 2012.
4. Société canadienne du sang. Déclaration des réactions indésirables, 2020. https://professionaleducation.blood.ca/fr/transfusion/publications/reactions-indesirables.
5. Callum J, Pinkerton P, Lima A, Lin Y, Karkouti K, Lieberman L, Pendergrast J, Robitaille N, Tinmouth A, Webert K. Réactions transfusionnelles. Clarke G et Chargé S (dir.) Guide de la pratique transfusionnelle. ProfessionalEducation.blood.ca/fr, Société canadienne du sang, 2017. https://professionaleducation.blood.ca/fr/reactions-transfusionnelles.
6. TRIP Foundation. Trip Report 2018, Hemovigilance - Extended Version, 2018, p. 40. https://www.tripnet.nl/wp-content/uploads/2020/08/Trip.HEMO_uitgebreid_ENGdef2020-4.pdf.
7. Serious Hazards of Transfusion-SHOT. Annual Shot Reports. https://www.shotuk.org/shot-reports/
8. Agence de la santé publique du Canada, Centre de lutte contre les maladies transmissibles et les infections. Système de surveillance des incidents transfusionnels (SSIT) : Résultats sommaires 2009-2013, 2016. https://www.canada.ca/fr/sante-publique/services/publications/medicaments-et-produits-sante/systeme-surveillance-incidents-transfusionnels-ssit-resultats-sommaires-2009-2013.html (Dernière consultation : 8 janvier 2021).
9. Yasui K, Matsuyama N, Takihara Y, Hirayama F. New Insights into Allergic Transfusion Reactions and Their Causal Relationships, Pathogenesis, and Prevention. Transfusion 2020; 60: 1590-601. https://onlinelibrary.wiley.com/doi/abs/10.1111/trf.15845.
10. Shimada E, Tadokoro K, Watanabe Y, Ikeda K, Niihara H, Maeda I, Isa K, Moriya S, Ashida T, Mitsunaga S, Nakajima K, Juji T. Anaphylactic Transfusion Reactions in Haptoglobin-Deficient Patients with Ige and Igg Haptoglobin Antibodies. Transfusion 2002; 42: 766-73. https://onlinelibrary.wiley.com/doi/abs/10.1046/j.1537-2995.2002.00117.x.
11. Koda Y, Watanabe Y, Soejima M, Shimada E, Nishimura M, Morishita K, Moriya S, Mitsunaga S, Tadokoro K, Kimura H. Simple Pcr Detection of Haptoglobin Gene Deletion in Anhaptoglobinemic Patients with Antihaptoglobin Antibody That Causes Anaphylactic Transfusion Reactions. Blood 2000; 95: 1138-43.
12. Savage WJ, Tobian AA, Fuller AK, Wood RA, King KE, Ness PM. Allergic Transfusion Reactions to Platelets Are Associated More with Recipient and Donor Factors Than with Product Attributes. Transfusion 2011; 51: 1716-22. https://onlinelibrary.wiley.com/doi/abs/10.1111/j.1537-2995.2010.03009.x.
13. Sandler SG, Eder AF, Goldman M, Winters JL. The Entity of Immunoglobulin a-Related Anaphylactic Transfusion Reactions Is Not Evidence Based. Transfusion 2015; 55:199-204. https://www.ncbi.nlm.nih.gov/pubmed/25066014.
14. Palmer DS, O’Toole J, Montreuil T, Scalia V, Yi QL, Goldman M, Towns D. Screening of Canadian Blood Services Donors for Severe Immunoglobulin a Deficiency. Transfusion 2010; 50: 1524-31. https://www.ncbi.nlm.nih.gov/pubmed/20158683.
15. Palmer DS, O’Toole J, Montreuil T, Scalia V, Goldman M. Evaluation of Particle Gel Immunoassays for the Detection of Severe Immunoglobulin A Deficiency and Anti-Human Immunoglobulin A Antibodies. Transfusion 2012; 52: 1792-8. https://onlinelibrary.wiley.com/doi/abs/10.1111/j.1537-2995.2011.03513.x.
16. Thibault L, Beauséjour A, De Grandmont MJ, Long A, Goldman M, Chevrier M-C. Establishment of an Immunoglobulin A-Deficient Blood Donor Registry with a Simple in-House Screening Enzyme-Linked Immunosorbent Assay. Transfusion 2006; 46 : 2115-21. https://onlinelibrary.wiley.com/doi/abs/10.1111/j.1537-2995.2006.01037.x.
17. O’Brien S. Rapport de surveillance 2019, Société canadienne du sang. https://professionaleducation.blood.ca/fr/transfusion/publications/rapport-de-surveillance (Dernière consultation : 3 mai 2021).
18. Héma-Québec. Comité d’hémovigilance du Québec, Rapport 2008. https://publications.msss.gouv.qc.ca/msss/fichiers/2009/09-212-05.pdf (Dernière consultation : 8 janvier 2021).
19. Tacquard C, Boudjedir K, Carlier M, Muller J-Y, Gomis P, Mertes PM. Hypersensitivity Transfusion Reactions Due to Iga Deficiency Are Rare According to French Hemovigilance Data. Journal of Allergy and Clinical Immunology 2017; 140: 884-5. https://doi.org/10.1016/j.jaci.2017.03.029.
20. Winters JL, Moore SB, Sandness C, Miller DV. Transfusion of Apheresis Plts from Iga-Deficient Donors with Anti-Iga Is Not Associated with an Increase in Transfusion Reactions. Transfusion 2004; 44: 382-5. https://onlinelibrary.wiley.com/doi/abs/10.1111/j.1537-2995.2003.00662.x.
21. Sandler SG. How I Manage Patients Suspected of Having Had an Iga Anaphylactic Transfusion Reaction. Transfusion 2006; 46: 10-3. https://onlinelibrary.wiley.com/doi/abs/10.1111/j.1537-2995.2006.00686.x.
22. Lilic D, Sewell WAC. Iga Deficiency: What We Should—or Should Not—Be Doing. Journal of Clinical Pathology 2001; 54: 337-8. https://jcp.bmj.com/content/jclinpath/54/5/337.full.pdf.
23. Sandler SG, Vassallo RR. Anaphylactic Transfusion Reactions. Transfusion 2011; 51: 2265-6. https://onlinelibrary.wiley.com/doi/abs/10.1111/j.1537-2995.2011.03404.x.
24. Hansen AL, Turner TR, Kurach JD, Acker JP. Quality of Red Blood Cells Washed Using a Second Wash Sequence on an Automated Cell Processor. Transfusion 2015; 55 : 2415-21. http://www.ncbi.nlm.nih.gov/pubmed/25988774.