Rapport de surveillance 2020
Nous sommes heureux de présenter ce rapport portant sur la surveillance des maladies infectieuses transmissibles par le sang. Une surveillance exercée de façon rigoureuse et en temps opportun est indispensable à la sécurité des réserves de sang. Cette surveillance comprend un suivi des marqueurs de maladies transmissibles faisant l’objet de tests de dépistage (notamment les infections bactériennes), des enquêtes sur les signalements d’infections possiblement transmises par transfusion ainsi que des analyses prospectives visant à déceler tout agent pathogène susceptible de constituer un risque.
Pour demander d’anciens rapports de surveillance, veuillez communiquer avec nous par l’entremise de notre formulaire.
Présent rapport : 2023
Rapports précédents : 2021, 2022
Rapport de surveillance 2020
Auteur : Sheila O'Brien, RN, PhD
Mise en ligne : août 2021
Résumé
Le présent rapport annuel porte sur la surveillance des maladies infectieuses transmissibles par le sang et des menaces émergentes. Une surveillance exercée de façon rigoureuse et en temps opportun est indispensable à la sécurité des réserves de sang. Cette surveillance comprend un suivi des marqueurs de maladies transmissibles détectables dans le sang, des enquêtes sur les signalements de transmission éventuelle par transfusion ainsi que des analyses prospectives visant à déceler tout agent pathogène susceptible de constituer un risque. Le rapport porte également sur la surveillance des risques de nature non infectieuse liés à certains aspects de la santé et de la sécurité des donneurs, ainsi que sur les services diagnostiques.
Surveillances des risques infectieux
Pour déceler les composants sanguins infectieux et empêcher leur transfusion aux patients, nous utilisons les tests de dépistage d’agents pathogènes les plus à jour. En 2020, le taux de maladies transmissibles pour 100 000 dons est demeuré très bas : 0 pour le virus de l’immunodéficience humaine (VIH); 5 pour le virus de l’hépatite C (VHC); 5 pour le virus de l’hépatite B (VHB); 0,9 pour le virus T-lymphotrope humain (HTLV) et 9,8 pour le virus de la syphilis. Des tests de dépistage sélectif de donneurs exposés à un risque d’infection par la maladie de Chagas n’ont révélé aucun don contaminé, et il y a eu 12 résultats positifs au test de dépistage du virus du Nil occidental (VNO). Selon les estimations actuelles, les risques résiduels d’infection par transfusion de sang potentiellement contaminé sont très faibles au Canada : 1 sur 12,9 millions de dons pour le VIH, 1 sur 27,1 millions de dons pour le VHC et 1 sur 2 millions de dons pour le VHB. Les enquêtes de retraçage de receveurs et de donneurs n’ont révélé aucune infection par transfusion. Une croissance bactérienne a été détectée dans 175 produits plaquettaires. Parmi les 114 donneurs potentiels de cellules souches ou de moelle osseuse testés, aucun n’a eu un résultat positif à un quelconque marqueur de maladies transmissibles. Des 283 échantillons de cellules souches provenant de mères qui ont fait un don de sang de cordon (sang contenu dans le cordon ombilical et le placenta) après leur accouchement, aucun n’a donné un résultat positif à l’un des marqueurs.
Les analyses prospectives visent à déterminer les menaces pour l’approvisionnement en sang. Le risque de babésiose, une maladie due à un parasite véhiculé par les tiques, demeure sous surveillance. Le parasite, Babesia microti, semble être au premier stade de son installation à quelques endroits au Canada, en particulier au Manitoba. En ce qui concerne le paludisme (malaria), les personnes qui ont voyagé ou résidé dans des régions touchées sont temporairement écartées du don de sang en raison du risque associé à la maladie. Par ailleurs, une période de non-admissibilité de 3 semaines est appliquée à toute personne ayant voyagé dans une région autre que le Canada, les États-Unis et l’Europe afin de réduire le risque d’infections découlant de courts voyages, comme l’infection par le Zika. Ce critère a été élargi en 2020 pour inclure tout voyage à l’extérieur du Canada afin de réduire le risque d’exposition d’autres donneurs et des membres du personnel au virus responsable de la COVID-19.
COVID-19
En novembre 2019, un nouveau coronavirus (SRAS-CoV-2) a été découvert à Wuhan, dans la province de Hubei, en Chine. Le 11 mars 2020, l’Organisation mondiale de la Santé a déclaré que la COVID-19 était pandémique. Bien que le SRAS-CoV-2 ne soit pas transmissible par le sang, de nombreuses mesures ont été mises en place pour protéger les donneurs, les bénévoles et le personnel dans les milieux de collecte de sang. Depuis le mois de mai, la Société canadienne du sang a effectué des tests de détection des anticorps contre le SRAS-CoV-2 sur plus de 100 000 échantillons de sang dans le cadre d’une étude menée en partenariat avec le Groupe de travail sur l’immunité face à la COVID-19 à la demande du gouvernement du Canada. Les résultats ont révélé un taux de séroprévalence faible (moins de 2 % de donneurs), ce qui montre que la grande majorité des personnes testées demeurent vulnérables à l’infection par le SRAS-CoV-2. Il était important de connaître ces données pour permettre aux responsables de la santé publique de planifier des mesures de sécurité pour protéger les Canadiens. En 2021, cette étude permettra de suivre la réponse anticorps au déploiement de la vaccination et les infections naturelles.
Pour protéger la santé des donneurs, des bénévoles et du personnel et assurer la suffisance des réserves, la Société canadienne du sang a dû mettre rapidement des mesures en place. Ainsi, elle a modifié son Initiative pour le bien-être du donneur afin de réduire les points de contact pouvant constituer un risque de transmission de la COVID-19. Lancée en mars 2019, l’Initiative avait pour but de réduire le nombre de réactions vagales et d’aider les donneurs à se sentir bien après leur don, même si le prélèvement de sang provoque rarement une réaction grave. Suivant cette modification, le taux de réaction vasovagale n’a pas augmenté. Par ailleurs, des périodes d’attente ont été imposées aux voyageurs ayant eu la COVID-19 ou ayant été en contact avec une personne infectée, mais peu de donneurs ont été exclus (< 0,2 %). De plus, dans l’éventualité d’une baisse de la participation des donneurs et afin de réduire le nombre de refus et assurer la suffisance des réserves, le taux d’hémoglobine minimal a été abaissé de 125 g/l à 120 g/l pour les femmes et de 130 g/l à 125 g/l pour les hommes, de juillet à octobre. Le taux de refus est passé de 7 % à 3,2 % chez les femmes et de 1,5 % à 0,8 % chez les hommes durant cette période.
Services diagnostiques
Les Services diagnostiques de la Société canadienne du sang effectuent des tests prénataux ainsi que des analyses pour les patients ayant des besoins transfusionnels complexes. Plusieurs provinces font faire des tests prénataux pour toutes les femmes enceintes alors que d’autres les demandent seulement pour certaines femmes. En 2020, les Services diagnostiques ont détecté des anticorps anti-érythrocytaires chez 1 160 femmes enceintes (la présence de ces anticorps peut constituer un risque de maladie hémolytique du fœtus et du nouveau-né) et chez 1 430 patients, qui peuvent avoir besoin de produits sanguins particuliers.
1. Introduction
Préserver le sang des risques de contamination implique une approche multidimensionnelle. L’information en ligne destinée aux donneurs et les dépliants qu’ils doivent lire sur place avant de faire un don décrivent les facteurs de risque de maladies transmissibles et indiquent dans quels cas les gens doivent s’abstenir de faire un don. Avant de donner du sang, chaque donneur doit remplir un questionnaire médical qui comprend des questions sur les facteurs de risque de maladies transmissibles. Le donneur doit ensuite rencontrer un membre du personnel qualifié qui détermine s’il peut donner du sang. Tous les dons sont soumis au dépistage de marqueurs d’agents pathogènes transmissibles par transfusion : le VIH, le VHB, le VHC, le virus T-lymphotrope humain ou HTLV (virus qui peut entraîner une leucémie, quoique ces cas soient rares) et le virus de la syphilis. Pour ce qui est du VNO, tous les dons sont soumis à un test de dépistage pendant la période à risque, soit le printemps, l’été et l’automne; l’hiver, seules les personnes qui ont voyagé à l’étranger sont testées. Un test de dépistage de la maladie de Chagas (transmise par une piqûre d’insecte d’Amérique latine) est effectué pour les donneurs à risque. Des tests bactériologiques sont en outre réalisés pour tous les produits plaquettaires. Un nouveau coronavirus, le SRAS-CoV-2, qui cause la COVID-19 (une infection respiratoire), est apparu en 2020. Bien que le virus ne soit pas transmissible par transfusion, il a eu des répercussions sur les opérations, car il fallait protéger la sécurité des donneurs, des employés et des bénévoles, tout en continuant de répondre aux besoins des receveurs de sang. De plus, la collecte de données épidémiologiques sur la prévalence des anticorps dans notre population de donneurs au fil du temps a contribué à la prise de décisions relatives à la santé publique pendant la pandémie.
La surveillance comprend un contrôle des tests effectués pour dépister les maladies transmissibles chez les donneurs, des enquêtes sur les maladies infectieuses possiblement transmises aux transfusés ainsi que des analyses prospectives visant à déceler les nouveaux agents pathogènes. Il est également essentiel de surveiller la sécurité des donneurs. Bien que la surveillance soit effectuée en temps réel tout au long de l’année, la publication du bilan est souvent légèrement retardée par les différentes étapes de la vérification finale. Le présent rapport décrit l’approche adoptée par la Société canadienne du sang en matière de surveillance des agents pathogènes transmissibles par le sang, des menaces infectieuses et de la sécurité des donneurs et contient les données de l’année civile 2020.
2. Surveillance des donneurs de sang
La figure 1 présente le nombre de dons allogéniques (sang total, plaquettes et plasma- aphérèse) effectués par des donneurs existants et des primo-donneurs (personnes qui font un don de sang pour la première fois). La majorité des dons — 90,2 % — provenaient de donneurs existants; 9,8 % provenaient de primo-donneurs. La baisse du nombre de dons recueillis en 2020 s’explique en partie par l’annulation d’interventions chirurgicales due au SRAS-CoV-2.
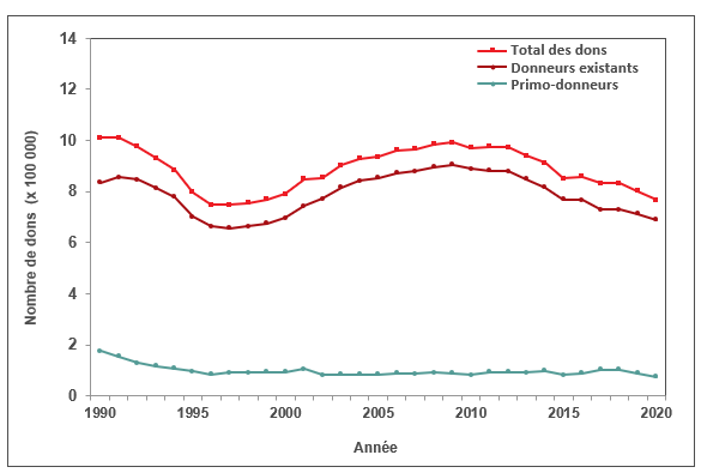
Figure 1. Nombre de dons effectués dans l’ensemble des régions desservies par la Société canadienne du sang, 1990-2020
Remarque : Les dons de plasma par aphérèse ne sont pas inclus dans ces données.
Agents pathogènes « classiques »
L’annexe 1 présente en détail les tests de dépistage utilisés et leur date d’entrée en vigueur. Le tableau 1 montre le nombre de dons infectés et les taux d’infection pour 100 000 dons par groupe démographique en 2020. La plupart du temps, les maladies transmissibles sont présentes chez les primo-donneurs; ces personnes n’ont été soumises à aucun dépistage auparavant et ont pu être infectées n’importe quand. Tous les dons porteurs d’agents infectieux transmissibles étaient des dons de sang total à l’exception d’un don par aphérèse déclaré positif pour le VHB. Il n’y a eu aucun don positif pour le VIH en 2020. Pour le VIH, le nombre de dons positifs a varié entre 1 et 4 par année au cours des cinq dernières années. Le taux d’infection pour 100 000 dons a diminué pour la plupart des marqueurs et le taux d’infection des dons des personnes ayant déjà fait un don est très bas (voir l’annexe 2). La seule exception est la syphilis, pour laquelle le taux d’infection est passé de 4,1 pour 100 000 dons en 2019 à 9,8 en 2020, et cette augmentation tend à être plus importante chez les donneurs réguliers que chez les primo-donneurs. Les cas de syphilis ont également augmenté dans la population générale, mais les deux situations ne sont pas directement comparables, car les cas enregistrés par la santé publique ne concernent que les personnes qui avaient des raisons de se faire tester (généralement les nouvelles infections avec symptômes) alors que les donneurs de sang comprennent à la fois les personnes qui ne sont pas conscientes de leur infection et celles qui ont pu être infectées dans le passé. Il est peu probable que la syphilis puisse être transmise par transfusion en raison des méthodes modernes de traitement du sang.
Tableau 1. Dons infectieux confirmés et taux de prévalence pour 100 000 dons, 2020
| Caractéristiques | Nombre de dons | Pourcentage de dons | VIH | VHC | VHB | HTLV | Syphilis | |||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Statut des donneurs | Pos | Taux | Pos | Taux | Pos | Taux | Pos | Taux | Pos | Taux | ||
|
Primo |
75 293 |
9,8 | 0 | - | 36 | 47,8 | 35 | 46,5 | 5 | 6,6 | 41 | 54,5 |
|
Existants |
690 516 | 90,2 | 0 | - | 2 | 0,3 | 3 | 0,4 | 2 | 0,3 | 34 | 4,9 |
| Sexe | ||||||||||||
|
Femme |
341 997 | 44,7 | 0 | - | 23 | 6,7 | 7 | 2,1 | 7 | 2,1 | 17 | 5,0 |
|
Homme |
423 812 | 55,3 | 0 | - | 15 | 3,5 | 31 | 7,3 | 0 | - | 58 | 13,7 |
| Âge | ||||||||||||
|
17-29 |
149 879 | 19,6 | 0 | - | 3 | 2,0 | 7 | 4,7 | 0 | - | 17 | 11,3 |
|
30-39 |
143 334 | 18,7 | 0 | - | 8 | 5,6 | 13 | 9,1 | 1 | 0,7 | 21 | 14,7 |
|
40-49 |
126 671 | 16,5 | 0 | - | 8 | 6,3 | 9 | 7,1 | 4 | 3,2 | 15 | 11,8 |
|
50+ |
345 925 | 45,2 | 0 | - | 19 | 5,5 | 9 | 2,6 | 2 | 0,6 | 22 | 6,4 |
| Total | 765 809 | 100 | 0 | - | 38 | 5,0 | 38 | 5,0 | 7 | 0,9 | 75 | 9,8 |
Toutes les unités contenant des agents pathogènes transmissibles sont détruites. Le plus grand risque provient de donneurs infectés juste avant de faire leur don : l’infection est alors trop récente pour être dépistée. La période pendant laquelle l’infection est indétectable est appelée « fenêtre sérologique ». Grâce aux techniques de dépistage actuelles, la fenêtre sérologique est très courte. Pour le VIH et le VHC, l’infection peut être dépistée dans les deux semaines suivant la contamination au moyen d’un test d’amplification des acides nucléiques (TAAN); pour le VHB, dans le mois qui suit. Le risque résiduel d’infection correspond à une estimation du risque qu’un don potentiellement infectieux soit transmis au cours de la fenêtre sérologique. Le tableau 2 contient les estimations basées sur les données de 2018 à 2 020. Le risque zéro n’existe pas, mais à l’heure actuelle, le risque est extrêmement faible.
Tableau 2. Estimation du risque résiduel d’infection par le VIH, le VHC et le VHB
| VIH | VHC | VHB |
|---|---|---|
| 1 don sur 12,9 millions | 1 don sur 27,1 millions | 1 don sur 2 millions |
Facteur de risque
Les donneurs qui obtiennent un résultat positif à un test de dépistage d’agents infectieux peuvent participer à un entretien afin de déterminer leurs facteurs de risque. Les principaux facteurs de risque sont présentés dans le tableau 3. Pour le VIH, il est difficile de généraliser, car les infections chez les donneurs sont très rares. La participation à ces entretiens étant volontaire, les données ne concernent que certains donneurs; chez de nombreux donneurs, aucun facteur de risque n’a pu être constaté.
Tableau 3. Facteurs de risque de maladies infectieuses chez les donneurs de sang
| Infection | Facteur de risque |
|---|---|
| VIH | Rapports hétérosexuels à haut risque Rapports sexuels entre hommes |
| VHC |
Antécédents de consommation de drogue par voie intravenineuse Être né en Afrique ou en Asie |
| VHB | Être né en Afrique ou en Asie |
| HTLV | Être né à l’étranger (surtout dans les Caraïbes) Antécédents de maladie transmissible sexuellement Antécédents de transfusion sanguine |
| Syphilis | Antécédents syphilitiques |
Remarque : Les donneurs ne participent pas tous à un entretien.
Maladie de Chagas (Trypanosoma cruzi)
La maladie de Chagas est provoquée par une infection parasitaire due à Trypanosoma cruzi (T. cruzi). On peut la contracter après avoir été piqué par un insecte surtout présent dans certaines régions du Mexique, d’Amérique centrale et d’Amérique du Sud. Le parasite T. cruzi peut également être transmis de la mère à l’enfant pendant la grossesse ainsi que par transfusion sanguine. Depuis que la Société canadienne du sang a commencé à réaliser des tests de dépistage chez les donneurs présentant des facteurs de risque en 2010, 35 dons infectés ont été recensés pour le T. cruzi (voir la figure 2). Sur les 9 201 dons analysés en 2020, aucun n’a produit un résultat positif.

Figure 2. Résultats des tests de dépistage de la maladie de Chagas, de 2010 à 2020
Virus du Nil occidental
Véhiculé par les moustiques, le virus du Nil occidental est présent en Amérique du Nord depuis 1999 (au Canada, depuis 2002). Bien que les symptômes puissent être graves, ils sont généralement modérés et la plupart des personnes infectées ne sont pas conscientes de l’être. Pendant le printemps, l’été et l’automne, les dons sont analysés par groupe de six, sous forme de mélange. Toutefois, les dons provenant des régions où le virus est actif — dons identifiés à l’aide d’un algorithme — sont analysés séparément, ce qui permet de réduire davantage les risques de contamination. En 2020, pendant la période où tous les dons sont analysés, c’est-à-dire le printemps, l’été et l’automne, sur 394 834 dons, 12 ont révélé un résultat positif; ces dons avaient été effectués entre le 4 août et le 7 septembre. Tous les dons positifs avaient été faits en Ontario, dans la région où on a identifié des cas cliniques. En ce qui concerne les dons effectués par des voyageurs pendant l’hiver (du 1er janvier au 31 mai et du 29 novembre au 31 décembre 2020), aucun n’a produit un résultat positif sur les 35 533 échantillons testés.

3. Surveillance des agents pathogènes émergents
Exercer une surveillance prospective des agents infectieux à diffusion hématogène présents dans la population générale nous permet de revoir rapidement nos politiques d’admissibilité des donneurs afin de préserver l’innocuité des produits sanguins. Comme nous surveillons les épidémies qui se déclarent dans d’autres parties du monde, nous sommes conscients des risques avant même que la maladie soit observée au Canada. Il est devenu banal de voyager à l’étranger et les maladies infectieuses peuvent rapidement se propager d’un pays à l’autre. Pour cerner les risques, la Société canadienne du sang doit disposer en tout temps des informations les plus récentes. Son personnel médical et scientifique obtient ces informations en s’affiliant à des organismes spécialisés en santé publique et en maladies infectieuses, et en exerçant une veille sur les sites Web et les revues qui publient le type de renseignements recherchés. S’il y a lieu, le cadre décisionnel fondé sur le risque, un outil élaboré par l’Alliance of Blood Operators (ABO), est utilisé pour faciliter la prise de décision. Cet outil permet de tenir compte de divers facteurs, notamment les risques infectieux pour les receveurs, l’impact opérationnel des stratégies envisagées, la perspective des parties prenantes et l’économie de la santé. Un certain nombre d’agents pathogènes présents au Canada et pouvant présenter un risque infectieux font l’objet d’une surveillance continue.
Maladie à coronavirus 2019 (COVID-19)
Le SRAS-CoV-2 est un nouveau coronavirus observé pour la première fois à Wuhan, dans la province chinoise du Hubei, à la fin de l’année 2019. Il s’agit du virus responsable d’une grave maladie respiratoire appelée maladie à coronavirus 2019 ou COVID-19. Certaines personnes infectées sont extrêmement malades et peuvent mourir à la suite de complications, tandis que d’autres n’éprouvent que de légers symptômes ou sont totalement asymptomatiques. Le 11 mars 2020, l’Organisation mondiale de la Santé a déclaré que la COVID-19 était pandémique. Depuis, près d’un million de Canadiens ont reçu un diagnostic de COVID-19 et 22 000 sont morts des suites de l’infection. Bien que le SRAS-CoV-2 ne soit pas transmissible par le sang, de nombreuses mesures ont été mises en place pour assurer la sécurité des donneurs et de l’approvisionnement en sang. Pour en savoir plus, consulter la section 8.
Séroprévalence du SRAS-CoV-2 (COVID-19)
Au début de la pandémie, lorsqu’il y avait moins de 500 cas confirmés au Canada (23 mars 2020), des mesures de distanciation physique rigoureuses ont été mises en place dans la plupart des provinces. Grâce à ces mesures, la première vague de la pandémie s’est stabilisée en juillet et en août après avoir atteint son pic à la fin d’avril. Les infections ont recommencé à augmenter vers la fin septembre 2020 et le virus a continué de se répandre dans l’ensemble du pays. Toutefois, le nombre de cas connus ne reflète pas le taux d’infection réel, car certaines personnes infectées ne développent pas la maladie et d’autres ne se sentent pas assez malades pour aller se faire tester. De plus, le dépistage se fait peut-être de façon disproportionnée là où il y a des éclosions. C’est pourquoi il est important d’effectuer des tests de détection des anticorps anti-SRAS-CoV-2 pour savoir quel pourcentage de la population a été infecté (la séroprévalence) et pour surveiller la séroprévalence tout au long de la pandémie. Les données recueillies peuvent aussi servir à améliorer les modèles mathématiques utilisés pour prédire le cours de l’infection et éclairer les politiques de santé publique. Ainsi, en partenariat avec le Groupe de travail du Canada sur l’immunité face à la COVID-19, la Société canadienne du sang analyse des échantillons de dons non utilisés pour détecter des anticorps contre le virus SRAS-CoV-2. Jusqu’ici, 124 976 échantillons de donneurs de partout au Canada ont été analysés. Les études sur la séroprévalence ont révélé que durant la première vague, la séroprévalence était inférieure à 1 %. Les taux ont augmenté au cours de la deuxième vague, mais sont demeurés relativement bas. La figure 3 montre les changements dans le temps.
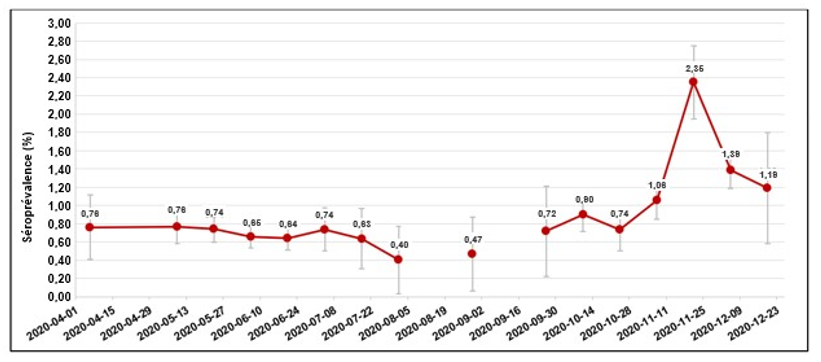
Figure 3. Estimations de la séroprévalence d’avril à décembre 2020.
Les points représentent les tendances à intervalles d’environ deux semaines et les barresreprésentent les intervalles de confiance à 95 %. Le dépistage a diminué à la fin de l’été et au début de l’automne, d’où une rupture dans la ligne.
À travers le monde, les fournisseurs de sang ont mis à contribution leur capacité opérationnelle pour éclairer les décisions en matière de santé publique. La séroprévalence du SRAS-CoV-2 est demeurée faible au Canada, mais des écarts significatifs ont été observés selon la région, l’origine ethnique et le statut socioéconomique. La Société canadienne du sang est déterminée à continuer de jouer un rôle central pour aider les autorités à évaluer les politiques de santé publique, surveiller les disparités et suivre la couverture vaccinale dans l’avenir.
Babésiose
La babésiose est causée par la piqûre d’une tique à pattes noires (Ixodes scapularis), qui peut transmettre le parasite Babesia microti. Elle provoque habituellement des symptômes pseudo- grippaux modérés et bien des gens ne savent même pas qu’ils en ont été porteurs. La maladie peut toutefois se transmettre par transfusion sanguine et provoquer chez les receveurs des symptômes graves ou même la mort. À ce jour, les cas de babésiose dans la population générale ont été recensés principalement dans le nord-est et le Haut-Midwest des États-Unis, où plus de 1 500 cas sont enregistrés chaque année. On estime qu’au total, plus de 200 infections signalées aux États-Unis auraient été transmises par transfusion. Au Canada, le parasite n’est présent que chez un petit nombre de tiques. Il y a eu un cas de transmission de la babésiose par voie transfusionnelle en 1998 par un donneur qui avait voyagé dans le nord-est des États-Unis. Dans le cadre d’une étude réalisée en 2013 par la Société canadienne du sang et Héma-Québec, 13 993 dons de sang ont été analysés et aucun ne s’est révélé positif. Cette même année, le cas d’une personne non donneuse qui a été infectée par une piqûre de tiques a été signalé au pays. D’après la surveillance continue des tiques par les autorités sanitaires, le risque n’a pas augmenté. En 2018, une étude a été menée auprès d’un plus grand nombre de donneurs : 50 752 échantillons provenant de régions du sud du pays ont été analysés et 1 a obtenu un résultat positif au test d’amplification des acides nucléiques (TAAN) pour B. microti (don effectué au Manitoba, résultat indiquant une infection active). Des 14 758 échantillons testés pour la présence d’anticorps dirigés contre B. microti, 4 provenant du sud-ouest de l’Ontario ont affiché un résultat positif (mais négatif au TAAN, ce qui permet de supposer que l’infection s’était résorbée). En 2019, une personne qui est tombée malade peu de temps après avoir donné du sang a reçu un diagnostic d’infection par B. microti. L’infection a probablement été contractée dans le sud du Manitoba. Aucun receveur n’a été infecté à cause de ce don. Le risque estimé de transmission par transfusion d’une infection cliniquement pertinente est très faible au Canada : 0,08 par année (0 – 0,38) ou environ 1 en 12,5 ans. Le cadre décisionnel d’ABO est utilisé pour mettre au point des stratégies d’atténuation des risques.
Virus de l'hépatite E (VHE)
L’hépatite E est une maladie courante dans les pays en développement, où elle se propage par l’eau et la nourriture contaminées. On l’associe également à la consommation de porc n’ayant pas été assez cuit. Elle est semblable à l’hépatite A et la plupart des personnes en bonne santé qui la contractent sont peu malades et guérissent sans même savoir qu’elles ont été infectées. Le virus de l’hépatite E peut toutefois rendre les personnes transfusées très malades. Dans une étude réalisée en 2013 par la Société canadienne du sang et Héma-Québec, 5,1 % des dons testés pour le virus de l’hépatite E ont révélé la présence d’anticorps (indiquant une infection antérieure par le virus), mais aucun n’a révélé la présence du virus comme tel. En 2015, dans le cadre d’une étude plus vaste, plus de 50 000 dons ont été soumis à un test plus sensible. Le taux de dons positifs pour le VHE s’est établi à 1 sur 4 615, mais la plupart des infections étaient à un stade tardif et le virus était en faible concentration, ce qui indique que les dons étaient peu susceptibles d’être infectieux. Moins élevé que dans certains pays d’Europe ayant des stratégies de dépistage, le risque présent au Canada est géré au moyen du cadre décisionnel fondé sur le risque, un outil mis au point par l’ABO. Il a été décidé de sensibiliser davantage la communauté médicale au VHE et de renforcer la surveillance des donneurs et des réactions indésirables.
Infections liées aux voyages à l’étranger
Les voyageurs peuvent ramener d’autres pays des infections transmissibles par le sang (figure 4). Le risque de contamination ne subsiste toutefois que pendant une certaine période après le retour au pays, le temps que l’organisme élimine l’agent pathogène du sang. Dans le cas de la malaria (paludisme), les risques sont présents dans certaines régions des Caraïbes, du Mexique, d’Amérique centrale, d’Amérique du Sud, d’Asie et d’Afrique. Les personnes qui reviennent de ces régions doivent attendre 3 mois avant de pouvoir donner du sang, soit suffisamment longtemps pour que les symptômes puissent se déclarer. Les personnes ayant résidé dans une région endémique doivent, elles, attendre pendant 3 ans, car il est possible qu’elles soient infectées depuis longtemps sans présenter de symptômes évidents. D’autres virus transmis par les moustiques, tels que celui de la dengue, sont présents depuis longtemps dans les régions touristiques tropicales fréquentées par les Canadiens, mais au cours des dernières années, on a observé aux Caraïbes, au Mexique, en Amérique centrale et en Amérique du Sud, l’éclosion de virus qu’on n’y voyait pas auparavant, à savoir le Chikungunya et le Zika. Selon des modèles d’évaluation quantitative des risques, les risques que ces virus contaminent le système d’approvisionnement en sang sont très faibles. Toutefois, en prévision des futurs risques infectieux liés aux voyages, la Société canadienne du sang a instauré en 2016 une période d’attente de 3 semaines applicable à toute personne ayant voyagé dans une région autre que le Canada, les États-Unis et l’Europe. Bien que la COVID-19 circule déjà au Canada, les infections liées aux voyages sont tout de même préoccupantes, en particulier celles découlant de nouveaux variants qui peuvent être rares au pays. Une période d’attente de 2 semaines a donc été mise en place pour tous les voyages à l’extérieur du Canada qui n’étaient pas visés par la période de non-admissibilité associée au risque d’infection par le Zika. Cela englobe les voyages aux États-Unis et en Europe.
Les séjours prolongés ou cumulatifs qui sont considérés comme un risque pour la transmission de la variante de la maladie de Creutzfeldt-Jakob (vMCJ) entraînent une exclusion à vie du don de sang. La vMCJ est associée à l’ingestion de bœuf infecté pendant l’épidémie d’encéphalopathie spongiforme bovine, ou ESB (« maladie de la vache folle »), qui a touché le Royaume-Uni, la France et d’autres pays européens. Sont donc exclues du don de sang les personnes qui ont résidé dans ces pays alors que de la viande contaminée était accessible à la consommation. Quant aux risques infectieux présents dans les autres pays, nous les surveillons de près afin de pouvoir réagir, le cas échéant.
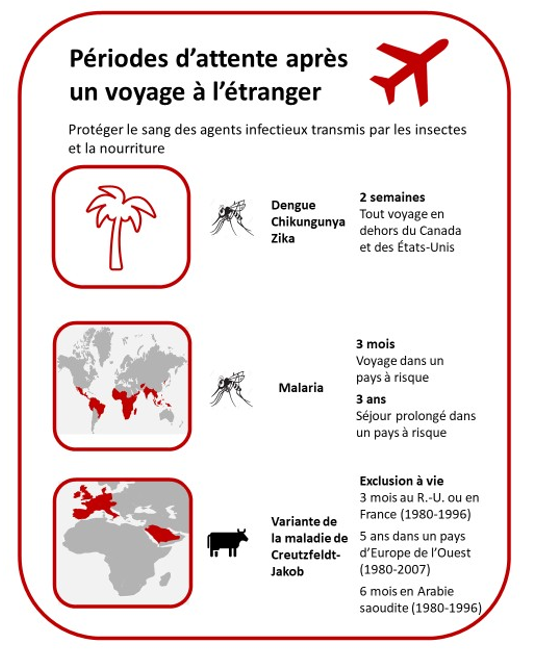
Figure 4. Principales périodes d’attente imposées pour réduire les risques de contamination.
4. Bactéries
Il y a des bactéries à la surface de la peau et ce sont généralement ces bactéries qui se retrouvent dans les dons de sang. Il arrive cependant que les bactéries présentes dans les produits sanguins proviennent du sang même des donneurs. Leur concentration, généralement faible au départ, peut atteindre des niveaux élevés dans les produits plaquettaires vu que ces produits sont entreposés à température ambiante. Cette prolifération bactérienne peut poser de sérieux risques pour les patients. C’est pour cette raison que la Société canadienne du sang soumet tous les mélanges de plaquettes et les plaquettes obtenues par aphérèse à un test de dépistage bactérien. Ce test est effectué au moyen du système BACT/ALERT, qui permet d’inoculer les échantillons en milieux aérobie (présence d’oxygène) et anaérobie (absence d’oxygène) et de surveiller la croissance bactérienne pendant 7 jours. Si une croissance bactérienne est observée, le produit qui est toujours dans les réserves de la Société canadienne du sang n’est pas distribué. Si le produit a déjà été expédié à un hôpital, il fait l’objet d’un rappel (s’il n’a pas encore été administré ou éliminé). En 2020, 105 720 produits plaquettaires (16 977 unités de plaquettes d’aphérèse et 88 743 mélanges de plaquettes) ont été testés; 97 unités de plaquettes d’aphérèse et 369 mélanges de plaquettes ont présenté une croissance bactérienne dans les flacons d’hémoculture. De ce nombre, 6 unités de plaquettes d’aphérèse et 118 mélanges de plaquettes ont montré une réelle contamination bactérienne. En outre, 12 unités de plaquettes d’aphérèse et 39 mélanges de plaquettes qui avaient donné des résultats positifs initiaux, sans confirmation par la suite, ont été transfusés, ou du moins délivrés. D’après les techniques d’analyse actuelles, cela représente une possibilité de contamination bactérienne (vrais positifs et positifs présumés) pour 175 produits, soit 16,6 produits sur 10 000.
5. Critères d’admissibilité au don de sang pour les hommes ayant des rapports sexuels avec des hommes
Dans les années 1980, afin de réduire les risques de transmission du VIH, il a été décidé que les hommes qui avaient eu des rapports sexuels avec d’autres hommes (HARSAH) depuis 1977, ne serait-ce qu’une seule fois, ne pouvaient pas donner de sang. Par la suite, les tests de dépistage et la surveillance des agents pathogènes émergents ont grandement été améliorés, de telle sorte que la période de non-admissibilité a été réduite à 5 ans en 2013, à 1 an en 2016, puis à 3 mois en 2019. Aucun de ces changements n’a fait augmenter le taux de VIH (figure 5). Un sondage anonyme a révélé que la réduction de la période de non- admissibilité a permis à un plus grand nombre de HARSAH de donner du sang et n’a eu aucune conséquence négative sur le respect des critères en vigueur (figure 5). Compte tenu des données enregistrées, le risque associé à la période d’attente de 3 mois a été estimé à 1 sur 34,2 millions de dons (1 sur 225 534 millions; 8,7 millions). Un autre sondage anonyme a été entrepris à la fin de 2020 afin d’évaluer les répercussions de la mise en œuvre de la nouvelle période d’attente de 3 mois. Beaucoup d’autres pays sont passés d’une exclusion à vie à une période de non-admissibilité restreinte, le plus souvent entre 3 mois et 1 an. Par exemple, en Angleterre, et depuis peu aux États-Unis, la période de non-admissibilité est de 3 mois, tandis qu’en France et aux Pays-Bas, elle est de 4 mois.
La Société canadienne du sang poursuit la révision de sa politique afin de trouver une façon de définir plus précisément le risque lié au comportement sexuel des donneurs plutôt que d’exclure tous les HARSAH sexuellement actifs. En janvier 2017, la Société canadienne du sang et Héma-Québec ont organisé une rencontre regroupant des chercheurs canadiens dans le domaine de la santé des hommes gais, des représentants d’autorités réglementaires (Santé Canada et la Food and Drug Administration des États-Unis), des parties prenantes et des experts internationaux. Les participants ont déterminé ensemble les domaines de recherche prioritaires pour évaluer la sécurité des produits en fonction de divers critères d’admissibilité potentiels. La Société canadienne du sang et Héma-Québec ont ensuite lancé un programme de subventions pour allouer à des chercheurs canadiens des sommes octroyées par Santé Canada. Quinze projets de recherche ont été subventionnés par voie de concours dans le cadre de ce programme. En 2020, un deuxième programme de subventions par voie de concours a été lancé. Également financé par Santé Canada, il est axé sur la recherche relative au don de plasma et aux HARSAH; quatre projets ont obtenu un financement. Consulter la page suivante pour en savoir plus : https://www.blood.ca/fr/recherche/nos-activites/nos-projects-de-recherche?combine=msm
Les résultats des études ont été présentés en novembre 2019 lors d’une rencontre à laquelle ont participé les bénéficiaires des subventions, des représentants de parties prenantes et d’autorités réglementaires (Santé Canada et la Food and Drug Administration des États-Unis), ainsi que des experts internationaux. Pour un complément d’information, consulter : https://www.blood.ca/fr/sang/puis-je-donner/hommes-ayant-eu-un-rapport-sexuel-avec-un- homme-harsah/rapport-provisoire-de-synthese-des-connaissances. En décembre 2020, les bénéficiaires des subventions se sont réunis à nouveau pour communiquer leurs résultats
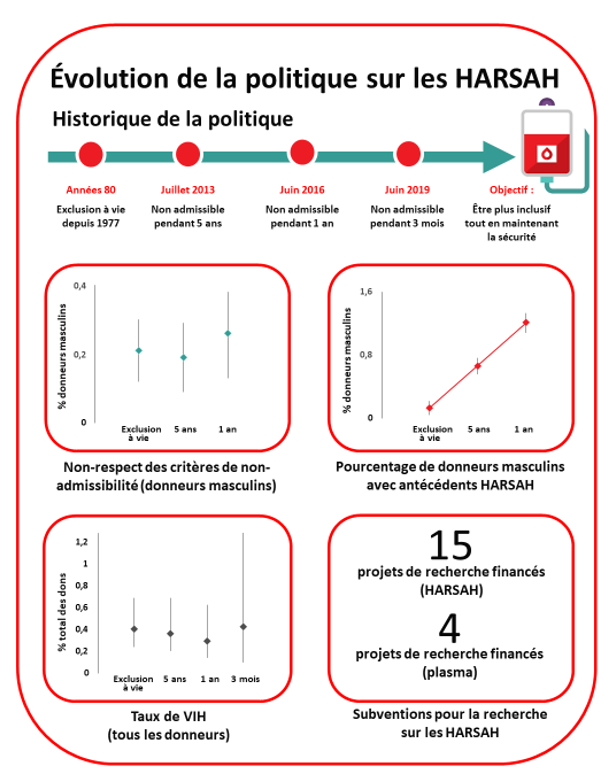
Figure 5. Le pourcentage de donneurs HARSAH a augmenté, mais la diminution des périodes de non-admissibilité n’a entraîné aucun changement dans le taux de non-respect de la politique ou le taux de VIH.
6. Retraçage des receveurs et des donneurs
Tous les cas de transmission d’infections possiblement associée à une transfusion font l’objet d’une enquête. Lorsqu’un donneur se révèle positif à un test de dépistage d’un agent infectieux ou qu’il nous signale, après le don, qu’il est atteint d’une infection transmissible par transfusion (même s’il ne s’agit pas d’une infection pour laquelle des tests sont normalement effectués), le programme de retraçage des receveurs et des donneurs en est informé. Un retraçage des receveurs est amorcé lorsqu’un don, qui vient d’être fait ou a été fait il y a longtemps, est identifié comme étant infecté. Les hôpitaux sont alors priés de communiquer avec les personnes ayant reçu les produits associés au don en question afin de les inviter à passer un test de dépistage. Le retraçage des donneurs est lancé lorsqu’on constate qu’un receveur a une infection transmissible et qu’une transfusion est confirmée. L’enquête de retraçage a alors pour but de déterminer si le receveur a contracté l’infection à cause de la transfusion. Les hôpitaux fournissent la liste de tous les produits sanguins que la personne a reçus et la Société canadienne du sang communique avec les donneurs concernés pour leur demander de passer un test de dépistage, à moins que les résultats des tests pertinents soient disponibles.
En 2020, 25 enquêtes ont été menées pour retracer des receveurs : 19 pour le dépistage du VHC, 3 pour le VHB, 2 pour le HTLV et 1 pour le VNO. Dix de ces enquêtes visaient des donneurs ayant obtenu un résultat positif à des tests internes, et 15 étaient associées à des tests externes ou à un avis de santé publique. De ces 25 enquêtes, 5 ont été fermées (tous les receveurs qui ont pu être joints ont été testés), et 20 sont toujours ouvertes. Par ailleurs, 10 enquêtes ouvertes dans les années précédentes ont été fermées en 2020. Aucune enquête close n’a été liée à une transmission par transfusion. Le nombre d’enquêtes pour retracer des receveurs à la suite de signalements de sources externes s’est élevé à 30 en 2020 : 2 cas de VIH, 25 cas de VHC et 3 cas de VHB. De ce nombre, 7 ont été fermées (tous les donneurs qui ont pu être joints ont été testés) et 23 sont encore ouvertes. En outre, 13 enquêtes ouvertes dans les années précédentes ont été closes. Aucune enquête close n’a été associée à une transmission d’un agent infectieux par transfusion.
7. Cellules souches sanguines
Les cellules souches peuvent se renouveler et se transformer en cellules sanguines (globules rouges, globules blancs ou plaquettes). Chez les adultes, ces cellules se trouvent surtout dans la moelle des gros os, mais on en trouve aussi, quoiqu’en moins grand nombre, dans la circulation sanguine. Le sang du cordon ombilical d’un nouveau-né en est riche. Les cellules sont prélevées du cordon ombilical et du placenta après la naissance d’un bébé en santé. Les cellules souches peuvent donc être extraites de la moelle osseuse, du sang circulant dans l’organisme (cellules souches du sang périphérique) ou du cordon ombilical (sang de cordon) après la naissance d’un bébé. Ces cellules jouent un rôle très important dans le traitement de diverses maladies comme les leucémies, les lymphomes et les myélomes multiples. La Société canadienne du sang a un programme national comprenant un registre de donneurs adultes et une banque de sang de cordon. Les tests de dépistage pratiqués sur tous les produits de cellules souches visent les mêmes marqueurs que pour le sang total.
Registre de donneurs de cellules souches de la Société canadienne du sang
Le Registre de donneurs de cellules souches de la Société canadienne du sang s’adresse aux Canadiens qui désirent donner des cellules souches de moelle osseuse ou de sang périphérique à toute personne qui pourrait en avoir besoin à un moment ou un autre. Le processus de qualification comprend un questionnaire portant sur les facteurs de risque d’infections transmissibles ainsi que le typage des antigènes leucocytaires humains ou HLA. En 2020, le registre comptait quelque 457 000 inscrits. Au total, 156 personnes ont été identifiées comme étant potentiellement compatibles avec un receveur et ont subi des tests additionnels, ce qui représente une diminution par rapport aux années précédentes. La pandémie de COVID-19 en est la cause principale, mais aussi le fait que l’on a choisi moins de personnes inscrites pour des patients étrangers en raison des restrictions de voyage limitant le transport des dons de cellules souches. Toutes les personnes inscrites qui ont été testées ont eu un résultat négatif pour tous les autres marqueurs de maladies infectieuses.
Banque de sang de cordon de la Société canadienne du sang
En 2020, la Banque de sang de cordon de la Société canadienne du sang a recueilli du sang de cordon dans quatre hôpitaux (Ottawa, Brampton, Edmonton, and Vancouver). Les femmes enceintes qui accouchent dans l’un de ces hôpitaux et souhaitent faire don du sang de cordon de leur nouveau-né doivent remplir un questionnaire médical et déclarer toute maladie transmissible ainsi que les facteurs de risque qui y sont liés. Si le don convient à une greffe (c’est-à-dire si la quantité de cellules souches est suffisante) et que tous les tests de dépistage ont donné des résultats négatifs, les cellules sont congelées et conservées jusqu’à ce qu’un patient en ait besoin. En 2020, sur les 283 échantillons de sang maternel testés, aucun n’a donné de résultat positif, quel que soit le marqueur. Encore une fois, ce chiffre est inférieur à ceux des années précédentes. Le contexte pandémique et la suspension des collectes dans les quatre hôpitaux durant la première moitié de l’année expliquent cette diminution.
8. Sécurité des donneurs
Réactions indésirables chez les donneurs
La Société canadienne du sang prend de nombreuses précautions pour le bien des donneurs : questionnaire médical, test d’hémoglobine, collation et surveillance après le prélèvement. Si la plupart des donneurs n’éprouvent aucun problème pendant ou après le don, il est néanmoins important de faire un suivi des incidents pour améliorer la prise en charge. Le tableau 4 présente une définition des différentes réactions indésirables pouvant survenir.
Tableau 4. Réactions et définitions
| Réactions | Définitions |
|---|---|
| Malaise vagal Modéré Grave |
Perte de conscience du donneur (évanouissement) Inconscience pendant moins de 60 secondes et aucune complication Inconscience pendant plus de 60 secondes ou complications |
| Incident cardiovasculaire important | Douleur thoracique ou infarctus du myocarde dans les 24 heures suivant le don; réaction pouvant être liée ou non au don |
| Resaignement | Saignement survenant spontanément au point de ponction après le don |
| Irritation nerveuse | Irritation ou lésion nerveuse durant le prélèvement, généralement décrite comme une douleur aiguë et lancinante, un picotement dans le bras ou un engourdissement |
| Inflammation/infection | Rougeur ou infection au point d’insertion de l’aiguille; se produit habituellement plusieurs jours après le don |
| Réaction allergique locale | Éruption cutanée causée par le pansement ou la solution utilisée pour nettoyer la peau; vésicules sur la peau |
| Douleur au bras | Douleur généralement due au brassard du tensiomètre, au garrot ou à la position du bras |
| Bleu/hématome | Coloration sombre temporaire de la peau due au saignement d’un vaisseau sanguin au moment du prélèvement |
| Ponction artérielle | Insertion de l’aiguille dans une artère au lieu d’une veine |
La figure 6 montre les taux de réaction enregistrés en 2020 pour 10 000 dons de sang total. Les résultats de 2019 sont indiqués à des fins de comparaison. Le taux de malaises vagaux modérés a diminué (p = 0,03), tout comme le taux de malaises graves, mais l’écart n’est pas statistiquement significatif (p > 0,05). Les gens les plus susceptibles de faire une réaction sont ceux qui font leur premier don, les jeunes donneurs (17 à 25 ans) et les femmes. Le système de déclaration des effets indésirables est orienté vers la saisie des réactions modérées et graves. La plupart du temps, les réactions sont légères; par exemple, des étourdissements ou un bleu au point d’insertion de l’aiguille. Toutefois, ces réactions ne sont consignées que si le donneur en fait mention à un moment donné après le don. Le tableau 5 présente la répartition des cas d’évanouissement (malaises modérés et graves) chez les donneurs de sang total selon le sexe et le type de donneur. Vu le petit nombre de donneurs dans chaque catégorie, les résultats ne diffèrent pas de façon significative de ceux rapportés en 2019 (p > 0,05), sauf en ce qui concerne les donneuses régulières chez qui une augmentation des blessures a été recensée en 2020 (p < 0,01).
En ce qui concerne les incidents cardiovasculaires, ils sont très rares et il est difficile de savoir si les incidents qui surviennent dans les 24 heures suivant un don sont liés au prélèvement ou s’il s’agit d’une coïncidence.
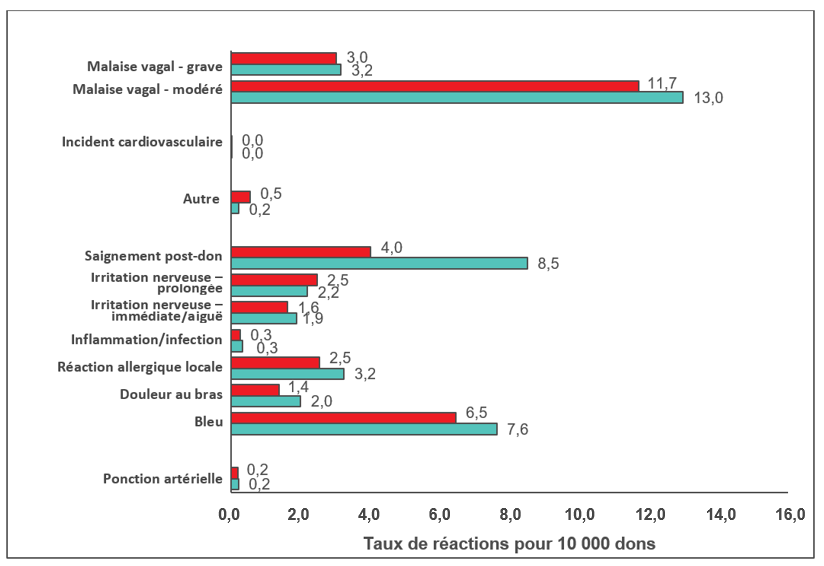
Figure 6. Taux de réactions pour 10 000 dons de sang total en 2020 (rouge) et en 2019 (vert)
Tableau 5. Évanouissements (malaises vagaux) en 2020 (sur 10 000 prélèvements)
| Malaises modérés et graves (tous)* | Malaises associés à une blessure*‡ | |||
|---|---|---|---|---|
| Type de don | Homme | Femme | Homme | Femme |
| Primo-donneur | 44,8 | 67,7 | 1,0 | 3,7 |
| Donneur existant | 5,0 | 17,1 | 0,3 | 1,8 |
| * Pour les malaises modérés et graves, toutes les comparaisons étaient statistiquement significatives (p < 0,05). Pour les malaises associés à une blessure, toutes étaient significatives, sauf pour les primo-donneurs vs les donneurs existants chez les hommes. ‡De façon générale, les malaises associés à une blessure n’étaient pas graves (bleus, coupures dues à une chute). |
||||
Depuis le début de la pandémie, les centres de donneurs ont continué d’offrir des collations aux donneurs après le don, mais afin de réduire le risque de transmission de la COVID-19, ceux-ci sont désormais invités à les prendre à l’extérieur du centre. Les collations salées et les bouteilles d’eau ne sont plus distribuées avant le prélèvement. Les donneurs sont encouragés à prendre une collation et à boire de l’eau avant leur arrivée au centre de donneurs. La distribution avant le don de collations salées et d’eau avait été instaurée en 2019, afin de réduire les malaises vagaux (évanouissements), tout comme la pratique d’exercices musculaires pendant le prélèvement. Ces exercices contribuent aussi à réduire le risque de malaise vagal. Ensemble, ces mesures font partie de l’Initiative pour le bien-être des donneurs. La figure 7 montre les taux de réaction avant la mise en place de l’Initiative, pendant son application et après l’arrêt de la distribution d’eau et de collations salées. On observe une baisse des malaises vagaux dans tous les groupes, mais cette tendance n’est significative que chez les donneurs existants (p < 0,01) et marginalement significative chez les donneuses existantes (p = 0,05). La modification des mesures de bien-être, qui visait à réduire le risque de transmission du virus responsable de la COVID-19, n’a entraîné aucun changement (p > 0,05).
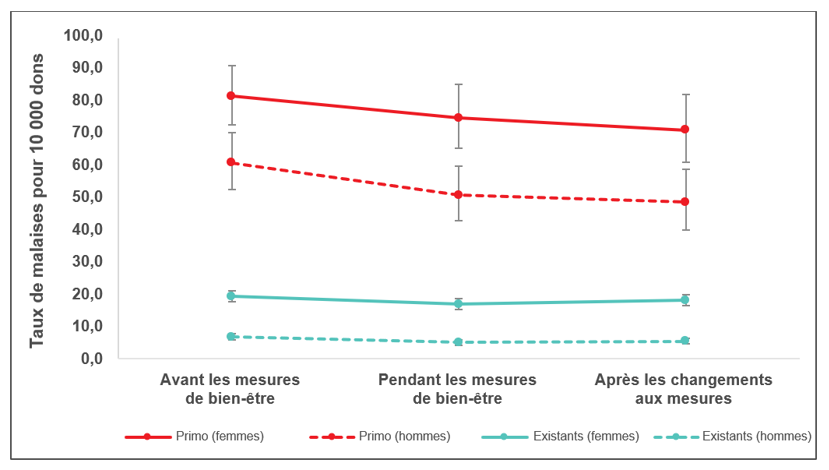
Figure 7. Malaises vagaux modérés et graves avant la mise en place des mesures de bien-être des donneurs (avril à décembre 2018), pendant l’application des mesures (avril à décembre 2019) et après la cessation des mesures découlant de l’instauration de mesures sanitaires liées à la COVID-19 (avril à décembre 2020).
COVID-19 et sécurité des donneurs
À l’heure actuelle, aucune donnée ne démontre que le SRAS-CoV-2 est transmissible par le sang. Il y a toutefois des inquiétudes sur deux plans : 1) la possibilité que des donneurs, des bénévoles et des employés puissent être infectés dans les centres de donneurs; 2) le risque de manquer de réserves de sang. En conséquence, des changements opérationnels ont été apportés. La figure 8 présente certaines des mesures auxquelles les donneurs doivent se conformer avant d’entrer dans un centre de donneurs et une fois qu’ils sont à l’intérieur. Dans la figure 9, on peut voir qu’un peu plus de 1 % des donneurs ont été refoulés au point de contrôle sanitaire qui précède le processus de sélection. Depuis mars, les personnes qui voyagent à l’extérieur du Canada doivent attendre deux semaines avant de pouvoir donner du sang (auparavant, l’attente était de trois semaines pour les voyages effectués ailleurs qu’au Canada, aux États-Unis et en Europe). Les donneurs qui ont eu la COVID-19 doivent attendre deux semaines après la disparition des symptômes. Pour ceux qui ont été en contact avec une personne infectée, la période de non-admissibilité est également de deux semaines. Plus tard, il a été décidé que les personnes qui avaient été hospitalisées pour la COVID-19 étaient écartées du don de sang pendant trois semaines après leur rétablissement. Le nombre de personnes qui ont pénétré dans un centre de donneurs et qui ont été renvoyées par la suite en raison de risques liés à la COVID-19 était également bas (0,2 %). La Société canadienne du sang a réussi à maintenir des niveaux suffisants de réserves de sang, qui sont demeurés supérieurs à la cible de janvier à décembre 2020 (figure 10). À certaines périodes de l’année, il y a eu une baisse de la demande, car des interventions chirurgicales non urgentes ont été annulées dans l’ensemble du Canada afin de libérer des ressources dans les hôpitaux pour le traitement des patients atteints de la COVID-19.
La figure 11 montre qu’il y a eu un peu moins de donneurs masculins pendant la pandémie de COVID-19, comparativement à la même période les deux années précédentes. Le nombre de primo-donneurs a encore baissé de manière similaire aux deux dernières années. La proportion de dons de jeunes donneurs (17 à 29 ans) a également diminué tandis que celle des donneurs de 50 ans et plus a augmenté, poursuivant toutes deux la tendance amorcée avant la COVID-19.
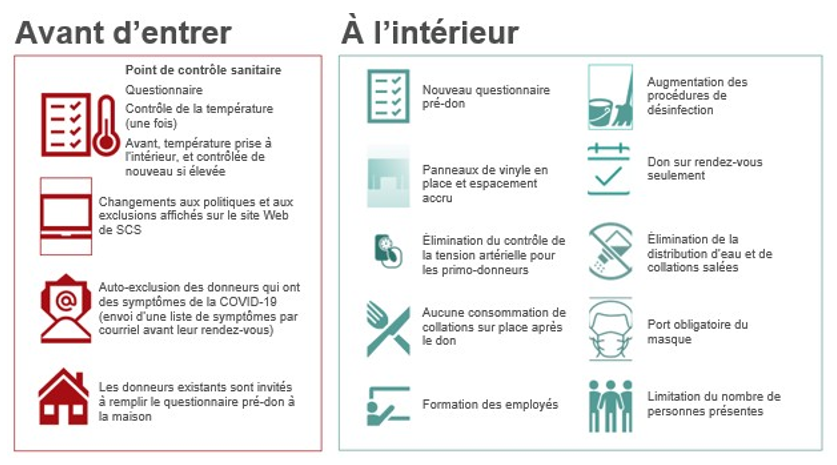
Figure 8. Principaux changements instaurés dans les lieux de collecte pour protéger les donneurs et le personnel pendant la pandémie de COVID-19
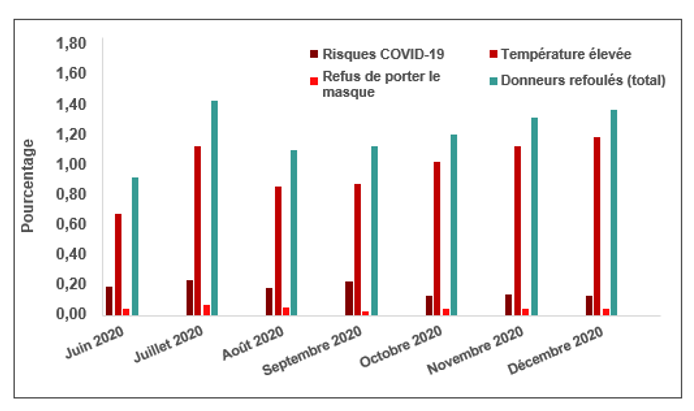
Figure 9. Pourcentage de donneurs refoulés à l’étape de la pré-sélection
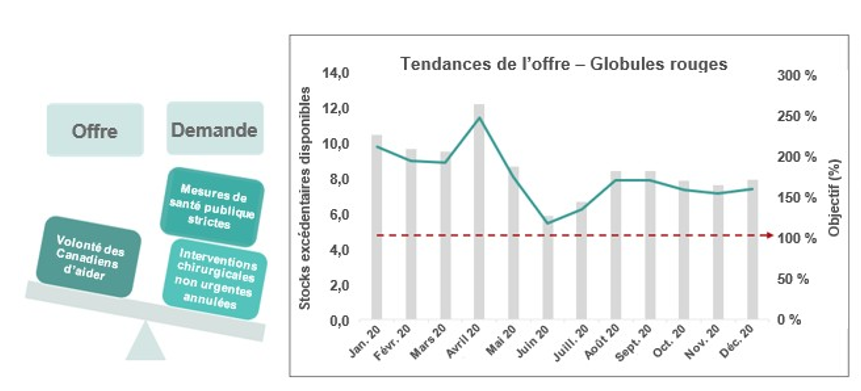
Figure 10. Facteurs influençant l’offre et la demande. Le but a toujours été de maintenir cinq jours de réserves de sang à la Société canadienne du sang (ligne pointillée rouge).
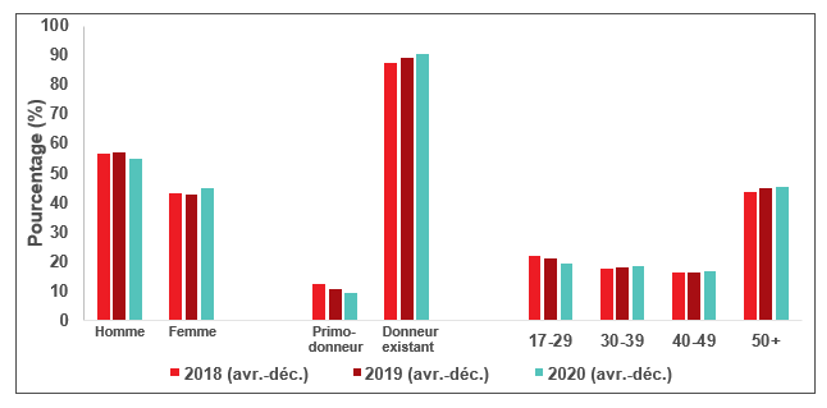
Figure 11. Dons avant la pandémie de COVID-19 (2018 et 2019) et pendant la pandémie, selon des variables démographiques
Taux d’hémoglobine et réserves de fer des donneurs
L’hémoglobine est la composante des globules rouges qui transporte l’oxygène. Comme elle est riche en fer, on associe généralement taux d’hémoglobine et réserves de fer. Un faible taux d’hémoglobine — raison la plus courante pour laquelle un donneur ne peut pas donner de sang — équivaut donc à de faibles réserves de fer. Des études réalisées à la Société canadienne du sang ont montré que les donneurs qui ont le plus souvent de faibles réserves de fer sont les femmes ainsi que les personnes qui donnent du sang souvent, que ce soient des hommes ou des femmes. Les donneurs masculins dont le taux d’hémoglobine est limite sont plus susceptibles d’avoir de faibles réserves de fer. Des mesures ont été adoptées en 2017 pour réduire les risques de carence en fer. Pour les femmes, l’intervalle minimal entre deux dons de sang total est passé de 56 à 84 jours. Cette période d’attente plus longue permet aux femmes de refaire leurs réserves de fer et de revenir à un taux normal d’hémoglobine. Afin de réduire le risque de pénuries de produits sanguins advenant une baisse des dons durant la pandémie, on a abaissé le taux d’hémoglobine minimal à 120 g/l pour les femmes et à 125 g/l pour les hommes, de juillet à octobre. Durant cette période, les taux de refus sont passés de 7 % à 3,2 % (p < 0,01) chez les femmes et de 1,5 % à 0,8 % (p < 0,01) chez les hommes.
Le site Web sang.ca contient de l’information sur le fer et la sécurité transfusionnelle, tout comme le dépliant Ce que vous devez savoir avant de donner du sang, que les donneurs sont tenus de lire avant chaque don.
9. Services diagnostiques
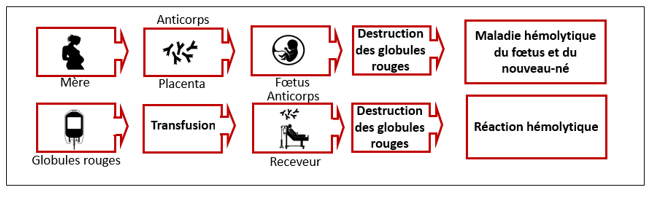
Les laboratoires de services diagnostiques analysent principalement le sang de femmes enceintes (analyses périnatales) et celui de patients devant recevoir des transfusions (analyses de compatibilité croisée et de référence). Certains laboratoires de la Société canadienne du sang fournissent tous les types de services.
| Maternel | 97,77 % |
| Paternel | 0,74 % |
| Sang de cordon | 1,49 % |
|
165 756 échantillons analysés |
Laboratoires d’analyses périnatales
Les laboratoires d’analyses périnatales fournissent des services de groupage sanguin et de recherche d’anticorps anti-érythrocytaires, dont certains peuvent causer la maladie hémolytique du fœtus et du nouveau-né. L’objectif de ces analyses est 1) d’identifier les femmes Rh négatif afin que puisse être recommandé un traitement permettant de prévenir l’apparition des anticorps anti-D, et 2) d’identifier les femmes possédant des anticorps problématiques afin qu’elles soient suivies et, au besoin, mises sous traitement. Les laboratoires réalisent aussi des analyses pour les pères, les nouveau-nés et les fœtus. En 2020, les analyses ont révélé 1 160 cas de femmes possédant des anticorps anti-érythrocytaires. La figure 12 montre les anticorps les plus communément susceptibles de présenter un risque pour le bébé.
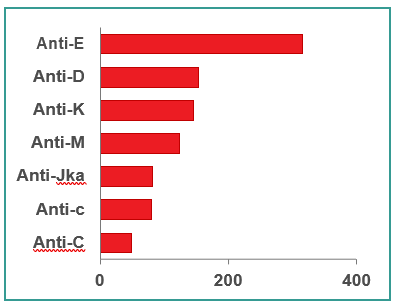
Figure 12. Types d’anticorps d’importance clinique et nombre de femmes enceintes chez qui chaque type d’anticorps a été détecté en 2020.
Laboratoires d’analyses de compatibilité croisée et de référence
Les laboratoires de référence fournissent des services d’analyses pour les patients nécessitant une compatibilité exacte entre leur groupe sanguin et celui du sang qui doit leur être transfusé. Ils réalisent également des recherches d’anticorps pour les patients possédant des anticorps anti-érythrocytaires inhabituels et présentant des besoins spéciaux en matière de compatibilité. La figure 13 montre le nombre de différents types d’anticorps identifiés chez les patients avant toute transfusion (1 430 patients). Il peut être difficile de trouver des produits sanguins appropriés pour les patients qui possèdent des anticorps ou antigènes rares. Le Laboratoire national de référence pour l’immunologie plaquettaire, à Winnipeg, au Manitoba, aide les professionnels de la santé dans la prise en charge des patients thrombopéniques en effectuant le typage HLA et HPA (antigènes plaquettaires humains) ainsi que des tests de détection d’anticorps anti-HLA et anti-HPA. Des plaquettes ayant fait l’objet d’un typage HLA et HPA sont disponibles pour le soutien transfusionnel de ces patients.
Pour en savoir plus, allez à blood.ca/en/hospital-services/laboratory-services/surveys.
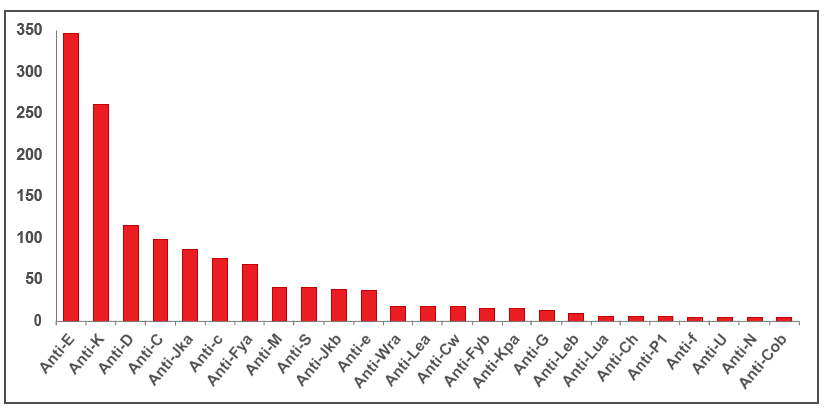
Figure 13. Nombre d’anticorps de référence identifiés en 2020
Bibliographie
Sélection des donneurs
Goldman M, Shih A W-Y, O’Brien SF, Devine D. Donor deferral policies for men who have sex with men: past, present and future. Vox Sang 2018; 113:95-103.
O’Brien SF, Osmond L, Fan W, Yi QL, Goldman M. Compliance with time based deferrals for men who have sex with men. Transfusion 2019; 59:916-920.
O’Brien SF, Goldman M, Robillard P, Osmond L, Myhal G, Roy E. Donor screening question alternatives to men who have sex with men time deferral: Potential impact on donor deferral and discomfort. Transfusion 2021; 61:94-101.
Saeed S, Goldman M, Uzicanin S, O’Brien SF. Evaluation of a Pre-exposure Prophylaxis (PrEP)/ Post Exposure Prophylaxis (PEP) Deferral Policy among Blood Donors. Transfusion 2021;doi:10.1111/trf.16349
Goldman M, Germain M, Gregoire Y, Vassallo RR, Kamel H, Bravo M, O’Brien SF. Safety of blood donation by individuals over age 70 and their contribution to the blood supply in five developed countries: a BEST Collaborative group study. Transfusion 2019; 59:1267-1272.
Risques résiduels
O’Brien SF, Yi Q-L, Fan W, Scalia V, Goldman M, Fearon MA. Residual risk of HIV, HCV and HVB in Canada. Transfus and Apher Sci 2017; 56:389-391.
O’Brien SF, Gregoire Y, Pillonel J, Steele WR, Custer B, Davison K, Germain M, Lewin A, Seed CR. HIV residual risk in Canada under a three-month deferral for men who have sex with men. Vox Sang 2020; 115:133-139.
Babesia microti
O’Brien SF, Delage G, Scalia V, Lindsay R, Bernier F, Dubuc S, Germain M, Pilot G, Yi QL, Fearon MA. Seroprevalence of Babesia microti infection in Canadian blood donors. Transfusion 2016; 56:237-243.
Tonnetti L, O’Brien SF, Gregoire Y, Proctor MC, Drews SJ, Delage G. Prevalence of Babesia in Canadian blood donors: June-October 2018. Transfusion 2019; 59:3171-3176.
Hépatite E
Fearon MA, O’Brien SF, Delage G, Scalia V, Bernier F, Bigham M, Weger S, Prabhu S, Andonov A. Hepatitis E in Canadian blood donors. Transfusion 2017; 57:1420-1425.
Delage G, Fearon M, Gregoire Y, Hogema BM, Custer B, Scalia V, Hawes G, Bernier F, Nguyen ML, Stramer S. Hepatitis E virus infection in blood donors and risks to patients in the United States and Canada. Trans Med Rev 2019; 33:139-145.
Bactéries
Ramirez-Arcos S, DiFranco C, McIntyre T, Goldman M. Residual risk of bacterial contamination of platelets: six years of experience with sterility testing. Transfusion 2017; 57:2174-2181.
Ramirez-Arcos S, Evand S, McIntyre T, Pang C, Yi QL, DiFranco C, Goldman M. Extension of platelet shelf life with an improved bacterial testing algorithm. Transfusion 2020; 60:2918-2928.
Paludisme
O’Brien SF, Ward S, Gallian P, Fabra C, Pillonel J, Davison K, Seed CR, Delage G, Steele WR, Leiby DA. Malaria blood safety policy in five non-endemic countries: a retrospective comparison through the lens of the ABO risk-based decision-making framework. Blood Transfus 2019; 17:94-102.
HTLV
O’Brien SF, Yi QL, Goldman M, Gregoire Y, Delage G. Human T-cell lymphotropic virus: A simulation model to estimate residual risk with universal leukoreduction and testing strategies in Canada. Vox Sang 2018; 113:750-759
Virus Zika
Germain M, Delage G, O’Brien SF, Grégoire Y, Fearon M, Devine D. Mitigation of the threat posed to transfusion by donors traveling to Zika-affected areas: a Canadian risk-based approach. Transfusion 2017; 57:2463-2468.
Murphy MS, Shehata N, Colas JA, Chassé M, Fergusson DA, O’Brien SF, Goldman M, Tinmouth A, Forster AJ, Wilson K. Risk of exposure to blood products during pregnancy: guidance for Zika and other donor deferral policies. Transfusion 2017; 57:811-815.
COVID-19
Saeed S, Drews SJ, Pambrun C, Yi QL, Osmond L, O’Brien SF. SARS-CoV-2 seroprevalence among blood donors after the first COVID-19 wave in Canada. Transfusion 2021; doi: 10.1111/trf.16296
Carence en fer
O’Brien SF, Goldman M. Understanding iron depletion and overload in blood donors. ISBT Science Series 2017; 12:11-18.
Goldman M, Uzicanin S, Osmond L, Scalia V, O’Brien SF. A large national study of ferritin testing in Canadian blood donors. Transfusion 2017; 57:564-570.
Goldman M, Yi QL, Steed T, O’Brien SF. Changes in minimum hemoglobin and interdonation interval: impact on donor hemoglobin and donation frequency. Transfusion 2019; 59:1734-1741.
Annexe I: Historique des tests de dépistage
| Marqueur | Entrée en vigueur* | |
|---|---|---|
| 1 | Syphilis | 1949 |
| 2 | Virus de l’hépatite B (VHB) | |
| AgHBs | 1972 | |
| Anticorps anti-HBc | 2005 | |
| Test d’amplification des acides nucléiques (TAAN) – VHB | 2011 | |
| 3 | Virus de l’immunodéficience humaine (VIH) | |
| ELISA (enzyme-linked immunosorbent assay) anti-VIH-1 | 1985 | |
| ELISA – anti-VIH-1/2 | 1992 | |
| Antigène p24 – VIH-1 | 1996 (supprimé en 2003) | |
| TAAN – VIH-1 | 2001 | |
| ELISA – anti-VIH-1/2 (dont le sous-type O du VIH-1) | 2003 | |
| 4 | Virus humain T-lymphotrope (HTLV) | |
| Anti-HTLV-II | 1990 | |
| Anti-HTLV-I/II | 1998 | |
| 5 | Virus de l’hépatite C (VHC) | |
| ELISA – anti-VHC | 1990 | |
| TAAN – VHC | 1999 | |
| 6 | Virus du Nil occidental (VNO) | |
| TAAN – VNO | 2003 | |
| 7 | Dépistage sélectif de la maladie de Chagas (Trypanosoma cruzi) | 2010 |
| 8 | Bactéries | |
| BacT/Alert | 2004 | |
| BacT/Alert modifié pour les plaquettes de sept jours | 2017 | |
| *Années d’entrée en vigueur des premiers dépistages, qui ont, depuis, évolué. | ||
Annexe II: Taux de prévalence du VIH, du VHC, du VHB, du HTLV et du virus de la syphilis dans les dons de primo-donneurs et de donneurs existants
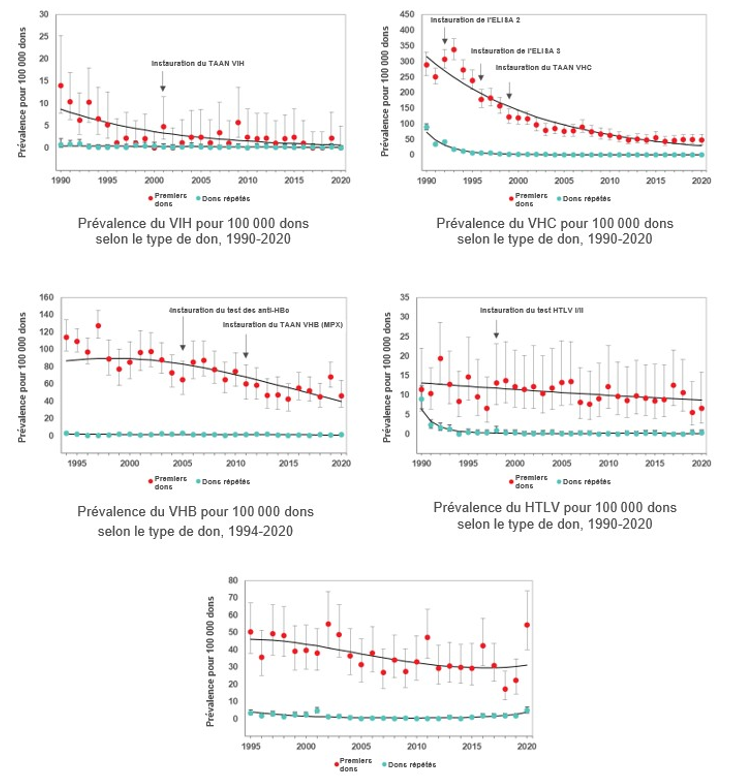
(Remarque : les échelles de ces graphiques diffèrent pour l’axe des y.)